题目内容
2.99℃时,Kw=1.0×10-12,该温度下测得0.1mol/LNa2A溶液的pH=6.下列说法不正确的是( )| A. | H2A在水溶液中的电离方程式为H2A=2H++A2- | |
| B. | 该温度下,将0.01mol/L的H2A溶液稀释20倍后溶液的pH=3 | |
| C. | 体积相同,pH均为1的盐酸和H2A溶液分别与足量的Zn反应,产生H2较多的是H2A | |
| D. | 将0.1mol/L的H2A溶液与0.2mol/L的氨水等体积混合后,溶液中浓度最大的离子是NH4+ |
分析 99℃时,Kw=1.0×10-12,则纯水中c(H+)=10-6mol/L,该温度下测得0.1mol/LNa2A溶液的pH=6,即c(H+)=10-6mol/L,溶液显中性,说明LNa2A不水解为强酸强碱盐,据此分析.
解答 解:A.99℃时,Kw=1.0×10-12,则纯水中c(H+)=10-6mol/L,该温度下测得0.1mol/LNa2A溶液的pH=6,即c(H+)=10-6mol/L,溶液显中性,则H2A为强酸,则H2A在水溶液中的电离方程式为H2A=2H++A2-,故A正确;
B.该温度下,将0.01mol/L的H2A溶液中氢离子浓度为0.02mol/L,稀释20倍,其后溶液的氢离子浓度为0.001mol/L,所以溶液的pH=3,故B正确;
C.盐酸和H2A均为强酸,完全电离,二者pH相同,则溶液中氢离子相同,所以与锌反应生成的氢气相同,故C错误;
D.将0.1mol/L的H2A溶液与0.2mol/L的氨水等体积混合后,二者恰好完全反应生成(NH4)2A,铵根离子只有小部分水解,所以溶液中浓度最大的离子是NH4+,故D正确.
故选C.
点评 本题考查了盐的水解、溶液中pH的简单计算、Kw在计算中的应用等,题目难度不大,侧重于考查学生对基础知识的综合应用能力,注意把握温度对水的离子积的影响.

练习册系列答案
相关题目
13.在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)?CO(g)+H2(g),若该化学平衡状态从正反应开始建立,达到平衡后,给平衡体系加压(缩小容积、其他条件不变),则容器内气体的平均相对分子质量将( )
| A. | 增大 | B. | 减小 | C. | 不变 | D. | 不能确定 |
7.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量的氨水溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2+3H2↑ |
14.某原电池装置图如图所示,有关该原电池的说法正确的是( )
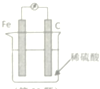

| A. | 在铁棒上产生气泡,碳棒上没有气泡 | |
| B. | H+在溶液中定向流向铁 | |
| C. | 电子由铁电极经导线流向碳棒 | |
| D. | 该装置能将电能转化为化学能 |
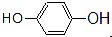 酚
酚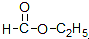 酯
酯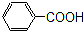 羧酸
羧酸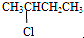 氯代烃
氯代烃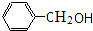 醇CH3C≡CH炔.
醇CH3C≡CH炔.