题目内容
化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成.有机物M(分子式:CxHySz)是隐形飞机上吸波材料的主要成分.
M充分燃烧的产物为三种氧化物,写出化学方程式: .
Ⅰ定性实验:
某化学兴趣小组为验证M组成元素进行了下列实验:将少量样品放入燃烧管A中,通入一定量O2,用电炉加热使其燃烧,所需装置如图所示(夹持仪器的装置已略去).
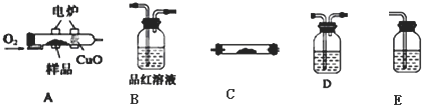
(1)该实验装置连接顺序为 .(上述每一组仪器只能使用一次)
(2)D中盛放的试剂是
(3)能证明有机物含碳元素的现象是 .
(4)燃烧管中放入CuO的作用是 .
(5)指出上述中错误的装置: .
Ⅱ定量实验:
(1)若测产生CO2气体体积,采用如图所示装置,实验结束后①调整量筒内外液面高度使之相同;②冷却至室温;③读取量筒内气体的体积.这三步操作的正确顺序是: (请填写步骤代号).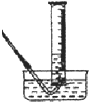
(2)若测产生CO2气体质量,采用沉淀法.下列沉淀剂最好的是
a.0.1mol/LCaCl2溶液 b.0.1mol/L Ca(OH)2溶液
c.0.1mol/L Ba(NO3)2 溶液 d.0.1mol/L Ba(OH)2溶液.
M充分燃烧的产物为三种氧化物,写出化学方程式:
Ⅰ定性实验:
某化学兴趣小组为验证M组成元素进行了下列实验:将少量样品放入燃烧管A中,通入一定量O2,用电炉加热使其燃烧,所需装置如图所示(夹持仪器的装置已略去).

(1)该实验装置连接顺序为
(2)D中盛放的试剂是
(3)能证明有机物含碳元素的现象是
(4)燃烧管中放入CuO的作用是
(5)指出上述中错误的装置:
Ⅱ定量实验:
(1)若测产生CO2气体体积,采用如图所示装置,实验结束后①调整量筒内外液面高度使之相同;②冷却至室温;③读取量筒内气体的体积.这三步操作的正确顺序是:

(2)若测产生CO2气体质量,采用沉淀法.下列沉淀剂最好的是
a.0.1mol/LCaCl2溶液 b.0.1mol/L Ca(OH)2溶液
c.0.1mol/L Ba(NO3)2 溶液 d.0.1mol/L Ba(OH)2溶液.
考点:探究物质的组成或测量物质的含量
专题:
分析:Ⅰ.有机物中C燃烧生成二氧化碳、氢生成水,硫生成二氧化硫,据此写出反应的化学方程式;
(1)实验原理是检验有机物完全燃烧时生成物有SO2、CO2和H2O,先检验水用无水硫酸铜,二氧化硫和二氧化碳都能使石灰水变浑浊,检验二氧化碳之前先检验二氧化硫,用品红检验即可,然后将二氧化硫用高锰酸钾来除去,然后将除净后再用石灰水检验二氧化碳;
(2)D的作用是除去二氧化硫并检验是否除净;
(3)检验二氧化碳之前先检验二氧化硫,用品红检验即可,然后将二氧化硫用高锰酸钾来除去,然后将除净后再用石灰水检验二氧化碳;
(4)氧化铜可以将生成的CO转化成CO2;
(5)没有排气管,会使容器内气压变大造成危险;
Ⅱ.(1)要准确测量气体体积必须保持量筒内外气体的温度和压强相等,因此在读取量筒内气体的体积之前,应使试管和量筒内的气体都冷却至室温;再调节量筒内外液面高度使之相同;
(2)考虑所选试剂浓度大,和二氧化碳反应生成沉淀多考虑.
(1)实验原理是检验有机物完全燃烧时生成物有SO2、CO2和H2O,先检验水用无水硫酸铜,二氧化硫和二氧化碳都能使石灰水变浑浊,检验二氧化碳之前先检验二氧化硫,用品红检验即可,然后将二氧化硫用高锰酸钾来除去,然后将除净后再用石灰水检验二氧化碳;
(2)D的作用是除去二氧化硫并检验是否除净;
(3)检验二氧化碳之前先检验二氧化硫,用品红检验即可,然后将二氧化硫用高锰酸钾来除去,然后将除净后再用石灰水检验二氧化碳;
(4)氧化铜可以将生成的CO转化成CO2;
(5)没有排气管,会使容器内气压变大造成危险;
Ⅱ.(1)要准确测量气体体积必须保持量筒内外气体的温度和压强相等,因此在读取量筒内气体的体积之前,应使试管和量筒内的气体都冷却至室温;再调节量筒内外液面高度使之相同;
(2)考虑所选试剂浓度大,和二氧化碳反应生成沉淀多考虑.
解答:
解:Ⅰ.有机物中C燃烧生成二氧化碳、氢生成水,硫生成二氧化硫,CxHySz燃烧的化学方程式4CxHySz+(4x+y+4z)O2
4xCO2+2yH2O+4zSO2;故答案为:4CxHySz+(4x+y+4z)O2
4xCO2+2yH2O+4zSO2;
(1)实验原理是检验有机物完全燃烧时生成物有SO2、CO2和H2O,先检验水用无水硫酸铜,选用C装置;二氧化硫和二氧化碳都能使石灰水变浑浊,检验二氧化碳之前先检验二氧化硫,用品红检验即可,选用B装置;然后将二氧化硫用高锰酸钾来除去,选用D装置;然后将除净后再用石灰水检验二氧化碳,选用E装置,
故答案为:A、C、B、D、E;
(2)检验二氧化碳之前应先除去二氧化硫并检验是否除净,故D中应放酸性高锰酸钾溶液,高锰酸钾具有强氧化性,可把二氧化硫氧化,若看到酸性高锰酸钾颜色变浅证明已除净,故答案为:酸性高锰酸钾溶液;
(3)碳元素燃烧产物是二氧化碳,二氧化碳可以用澄清石灰水来检验,检验二氧化碳之前先检验二氧化硫,用品红检验即可,然后将二氧化硫用高锰酸钾来除去,待除净后再用石灰水检验二氧化碳,
故答案为:D中溶液不褪色(或变浅),E中溶液变浑浊;
(4)氧化铜可以将碳元素不完全燃烧生成的CO转化成CO2,
故答案为:将有机物中的碳元素全部氧化成二氧化碳;
(5)装置F只有进气管没有排气管,会使容器内气压变大造成危险,
故答案为:装置E中试剂瓶未与空气相通;
Ⅱ.(1)停止加热、回到室温后,将量筒下移以调节量筒内的液面与水槽一致,此时量筒内气体压强也为大气压,读数才是正确的;所以正确的操作顺序为:②使气体都冷却至室温;①调整量筒内外液面高度使之相同;③读取量筒内气体的体积;即②①③;故答案为:②①③;
(2)氯化钙和硝酸钡和二氧化碳不反应,氢氧化钙溶解度小,得不到0.1mol/L溶液,氢氧化钡和二氧化碳反应生成碳酸钡沉淀,故选:d.
| 点燃 |
| 点燃 |
(1)实验原理是检验有机物完全燃烧时生成物有SO2、CO2和H2O,先检验水用无水硫酸铜,选用C装置;二氧化硫和二氧化碳都能使石灰水变浑浊,检验二氧化碳之前先检验二氧化硫,用品红检验即可,选用B装置;然后将二氧化硫用高锰酸钾来除去,选用D装置;然后将除净后再用石灰水检验二氧化碳,选用E装置,
故答案为:A、C、B、D、E;
(2)检验二氧化碳之前应先除去二氧化硫并检验是否除净,故D中应放酸性高锰酸钾溶液,高锰酸钾具有强氧化性,可把二氧化硫氧化,若看到酸性高锰酸钾颜色变浅证明已除净,故答案为:酸性高锰酸钾溶液;
(3)碳元素燃烧产物是二氧化碳,二氧化碳可以用澄清石灰水来检验,检验二氧化碳之前先检验二氧化硫,用品红检验即可,然后将二氧化硫用高锰酸钾来除去,待除净后再用石灰水检验二氧化碳,
故答案为:D中溶液不褪色(或变浅),E中溶液变浑浊;
(4)氧化铜可以将碳元素不完全燃烧生成的CO转化成CO2,
故答案为:将有机物中的碳元素全部氧化成二氧化碳;
(5)装置F只有进气管没有排气管,会使容器内气压变大造成危险,
故答案为:装置E中试剂瓶未与空气相通;
Ⅱ.(1)停止加热、回到室温后,将量筒下移以调节量筒内的液面与水槽一致,此时量筒内气体压强也为大气压,读数才是正确的;所以正确的操作顺序为:②使气体都冷却至室温;①调整量筒内外液面高度使之相同;③读取量筒内气体的体积;即②①③;故答案为:②①③;
(2)氯化钙和硝酸钡和二氧化碳不反应,氢氧化钙溶解度小,得不到0.1mol/L溶液,氢氧化钡和二氧化碳反应生成碳酸钡沉淀,故选:d.
点评:本题考查有机物组成的测定,题目难度中等,注意把握实验的原理和方法,明确实验操作目的是解答该题的关键,注意氢氧化钙微溶于水,用来检验二氧化碳,不能用来吸收二氧化碳.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
铊和铝属于同主族元素,关于铊的性质的推断可能错误的是( )
| A、铊是银白色,质软的金属 |
| B、铊位于第六周期第ⅢA族 |
| C、铊和稀硝酸反应生成Tl(NO3)3 |
| D、Tl(OH)3和Al(OH)3一样是两性氢氧化物 |
化学概念在逻辑上存在如图所示关系:对下列概念相互关系的说法中正确的是( )
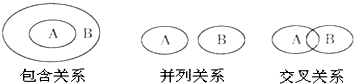

| A、纯净物与混合物属于包含关系 |
| B、化合物与电解质属于包含关系 |
| C、单质与化合物属于交叉关系 |
| D、氧化还原反应与化合反应属于并列关系 |
下列反应中可判断为可逆反应的是( )
| A、氢气和氯气点燃生成氯化氢,氯化氢受热分解为氢气和氯气 |
| B、氮气和氢气在高温、高压、催化剂作用下可以生成氨气,同时氨气又分解为氮气和氢气 |
| C、单质溴可以置换出碘,氯气又可以置换出溴 |
| D、氯气和水反应生成盐酸和次氯酸,次氯酸光照条件下可分解为盐酸和氧气 |
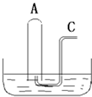 如图所示:在B槽中装有500mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中,充分反应,试管A中余下气体的体积为0.5amL.
如图所示:在B槽中装有500mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中,充分反应,试管A中余下气体的体积为0.5amL.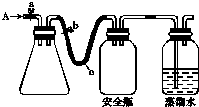 实验室用下列方法测定某水样中O2的含量.
实验室用下列方法测定某水样中O2的含量.