题目内容
17.不用任何试剂就能鉴别的一组物质是( )| A. | Na2CO3和NaHCO3 | B. | Na2CO3和NaCl | C. | Na2CO3和盐酸 | D. | NaHCO3和盐酸 |
分析 不用任何化学试剂就可以鉴别的物质可以采用相互滴加的方法检验,滴加顺序不同,现象不同的可以鉴别.
解答 解:A.Na2CO3和NaHCO3不反应,不加试剂不能鉴别,故A不选;
B.Na2CO3和NaCl不反应,不加试剂不能鉴别,故B不选;
C.盐酸少量不生成气体,盐酸过量生成气体,则Na2CO3和盐酸采用相互滴加的方法检验,故C选;
D.NaHCO3和盐酸的反应与量、滴加顺序无关,不加试剂不能鉴别,故D不选;
故选C.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意与量有关的离子反应,题目难度不大.

练习册系列答案
相关题目
7.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,1 L 1 mol•L-1的BaCl2溶液中有NA个Cl- | |
| B. | 1 mol Fe被完全氧化生成Fe3O4,失去8 NA个电子 | |
| C. | 常温常压下,14 g的CO和N2混合气体含有的原子数为NA | |
| D. | 常温常压下,22.4 L氧气与足量镁粉充分反应,转移的电子数为2NA |
8.CuO、Fe粉、Fe3O4的混合物中,加一定量稀硫酸,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,片刻后.取出铁钉,观察现象.以下结论中正确的是( )
| A. | 若铁钉部分溶解,则滤液中一定含Fe2(SO4)3 | |
| B. | 若铁钉完全溶解,则滤液中一定含CuSO4 | |
| C. | 若铁钉表面有红色物质生成,则不溶物中一定不含Fe | |
| D. | 若铁钉无变化,则不溶物中一定含Fe |
5.下列说法正确的是( )
| A. | 常温下,铁比铝更易生锈,说明铁比铝活泼 | |
| B. | 钠比铜活泼,将钠投入硫酸铜溶液中,会有红色的铜析出 | |
| C. | 镁粉中混有的少量铝粉,可加足量NaOH溶液过滤除去 | |
| D. | 从1L 0.5mol/L FeCl3溶液中取出100mL,其中Cl-浓度为0.15 mol/L |
2.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | NA个氢气分子所占的体积为22.4L | |
| B. | 常温下,22.4 L NO2中所含的氧原子数为2 NA | |
| C. | 14 g氮气所含的N原子数为NA | |
| D. | 标准状况下,22.4 L水所含的H2O分子数为NA |
9.在下列100mL液体中,分别加入0.05molNaOH晶体,溶液导电性变化较大的是( )
| A. | 0.5mol/L NH4Cl溶液 | B. | 0.5mol/L盐酸 | ||
| C. | 0.5mol/LH2SO4 | D. | 0.5mol/L醋酸 |
6.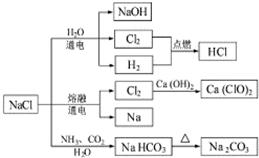 NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )
NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )
 NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )
NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )| A. | 25℃时,NaHCO3在水中的溶解度比Na2CO3的小 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下液氯能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应都是氧化还原反应 |
7.如表由实验现象得出的结论正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液加入盐酸,有无色无味气体产生 | 溶液一定含有CO32- |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液一定含Fe2+ |
| C | 向某溶液滴加浓NaOH溶液加热,有能使湿润的红色石蕊试纸变蓝的气体产生 | 溶液一定存在NH4+ |
| D | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管中有晶体凝结 | NH4Cl固体可以升华 |
| A. | A | B. | B | C. | C | D. | D |