题目内容
11.化合物F是一种重要的有机合成中间体,它的合成路线如图: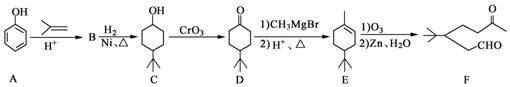
(1)化合物F中含氧官能团的名称是羰基 和醛基.
(2)通过实验可证明A物质具有极弱的酸性,写出有关的化学方程式
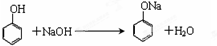 .
.(3)化合物B的结构简式为
 ,A到B的反应类型为加成反应.
,A到B的反应类型为加成反应.(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢.写出该化合物的结构简式
 (任写一种).
(任写一种).(5)请根据已有知识并结合相关信息,写出以苯酚(
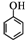 )和CH2=CH2为原料制备有机物 的
)和CH2=CH2为原料制备有机物 的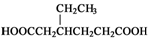 合成路线流程图(无机试剂任用).
合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$Br-CH2CH2-Br.
分析 根据题中各物质的转化关系可知,由A 到C
到C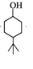 的变化分别是:在苯酚的对位上发生加成反应引入了一个烷烃基(丁基),然后苯环上发生与氢气的加成,变为环己烷,据此可以推断出B的结构简式为:
的变化分别是:在苯酚的对位上发生加成反应引入了一个烷烃基(丁基),然后苯环上发生与氢气的加成,变为环己烷,据此可以推断出B的结构简式为: ,然后C中醇羟基被氧化生成酮基,即得到D,E发生氧化反应生成F.
,然后C中醇羟基被氧化生成酮基,即得到D,E发生氧化反应生成F.
(5)苯酚和乙烯发生加成反应生成对羟基乙苯,对羟基乙苯发生加成反应生成4-乙基环己醇,4-乙基环己醇发生消去反应生成3-乙基环己烯,3-乙基环己烯发生氧化反应生成OHCCH2CH(CH2CH3)CH2CH2CHO,OHCCH2CH(CH2CH3)CH2CH2CHO发生氧化反应生成 .
.
解答 解:根据题中各物质的转化关系可知,由A 到C
到C 的变化分别是:在苯酚的对位上发生加成反应引入了一个烷烃基(丁基),然后苯环上发生与氢气的加成,变为环己烷,据此可以推断出B的结构简式为:
的变化分别是:在苯酚的对位上发生加成反应引入了一个烷烃基(丁基),然后苯环上发生与氢气的加成,变为环己烷,据此可以推断出B的结构简式为: ,然后C中醇羟基被氧化生成酮基,即得到D,E发生氧化反应生成F.
,然后C中醇羟基被氧化生成酮基,即得到D,E发生氧化反应生成F.
(1)F中官能团为羰基和醛基,故答案为:羰基、醛基;
(2)苯酚能和碱反应生成盐和水而证明苯酚具有酸性,如和NaOH溶液反应生成可溶性的苯酚钠,反应方程式为 ,
,
故答案为: ;
;
(3)通过以上分析知,B结构简式为 ,A发生加成反应生成B,
,A发生加成反应生成B,
故答案为: ;加成反应;
;加成反应;
(4)D的分子式为:C10H18O,某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢,故此有机物满足对称结构即可,可以为: 等,
等,
故答案为: ;
;
(5)要以苯酚(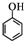 )和CH2=CH2为原料制备有机物
)和CH2=CH2为原料制备有机物 ,可以先用苯酚与乙烯加成反应生成对乙基苯酚,对乙基苯酚加成生成对乙基环己醇,对乙基环己醇消去生成3-乙基环己烯,3-乙基环己烯氧化生成产物,故流程为:
,可以先用苯酚与乙烯加成反应生成对乙基苯酚,对乙基苯酚加成生成对乙基环己醇,对乙基环己醇消去生成3-乙基环己烯,3-乙基环己烯氧化生成产物,故流程为: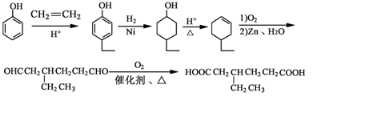 ,
,
故答案为: .
.
点评 本题考查有机合成,为高频考点,根据反应前后结构简式变化确定反应类型,侧重考查学生分析判断及合成路线设计能力,需要学生熟练掌握常见有机反应类型、反应条件,难点是(5)题路线设计.

| A. | 室温下,1L pH=13的氢氧化钡溶液所含OH- 数为0.2NA | |
| B. | 标准状况下,0.1molAl3+含有的核外电子数为0.3 NA | |
| C. | 常温下,44gCO2中含有2NA个碳氧双键 | |
| D. | 将1 molN2 和3mol H2 通入密闭容器中,一定条件下充分反应,转移电子数为6NA |
| A. | Cu(OH)2和盐酸; Cu(OH)2和CH3COOH | |
| B. | BaCl2和Na2SO4; Ba(OH)2和CuSO4 | |
| C. | NaHCO3和NaHSO4 Na2CO3和NaHSO4 | |
| D. | NaHCO3( 过量)和Ca(OH)2 Ca(HCO3)2 和NaOH( 过量) |
| A. | 醋酸钠中加入盐酸:CH3COONa+H+→CH3COOH+Na+ | |
| B. | 在硫酸作催化剂、加热条件下乙烯与水发生加成反应:CH2═CH2+H2O $→_{△}^{H_{2}SO_{4}}$ CH3CH2OH | |
| C. | 甲醛溶液中加入足量的银氨溶液并加热: HCHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$HCOO-+NH4++2Ag↓+3NH3+H2O | |
| D. | 2分子甘氨酸 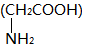 在一定条件下脱去2分子水: 在一定条件下脱去2分子水: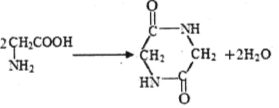 |
(1)已知反应CO(g)+2H2(g)?CH3OH(g)△H=-99kJ•mol-1中的相关化学键能如表:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | x | 465 | 413 |
(2)甲醇作为一种重要的化工原料,既可以作为燃料,还可用于合成其它化工原料.在一定条件下可利用甲醇羰基化法制取甲酸甲酯,其反应原理可表示为:CH3OH(g)+CO(g)?HCOOCH3(g)△H=-29.1kJ•mol-1.向体积为2L的密闭容器中充入2mol CH3OH(g) 和2mol CO,测得容器内的压强(p:kPa)随时间(min)的变化关系如图1中Ⅰ、Ⅱ、Ⅲ曲线所示:

①Ⅱ和Ⅰ相比,改变的反应条件是使用催化剂.
②反应Ⅰ在5min时达到平衡,在此条件下从反应开始到达到平衡时v(HCOOCH3)=0.10mol•L-1•min-1.
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=2L•mol-1.在体积和温度不变的条件下,在上述反应达到平衡Ⅱ时,再往容器中加入1mol CO和2mol HCOOCH3后v(正)< v(逆) (填“>”“<”“﹦”),原因是浓度商Qc=$\frac{1.5}{0.5•1}$=3>2=K反应向逆方向进行,故v(正)<v(逆).
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1>T3(填“>”“<”“﹦”),判断的理由是此反应为放热反应,降温,平衡向正向进行(或反应Ⅰ达平衡时所需的时间比反应Ⅲ达平衡时所需的时间短,反应速率快,故T1温度更高).
(3)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2.某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如图2所示,利用以下反应填空:
NO+CO?N2+CO2(有CO) 2NO?N2+O2(无CO)
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为此反应为放热反应,升高温度反应更有利于向逆反应方向进行.
②在$\frac{n(NO)}{n(CO)}$=1的条件下,应控制最佳温度在870℃左右.
 溶液加入到120mL盐酸中,所得溶液的pH为2。如果混合前氢氧化钠溶液和盐酸的物质的量浓度相同,它们的浓度是 ( )
溶液加入到120mL盐酸中,所得溶液的pH为2。如果混合前氢氧化钠溶液和盐酸的物质的量浓度相同,它们的浓度是 ( )

 ≈4.0]。
≈4.0]。