题目内容
下列说法不正确的是( )
| A、从HCl、HBr到HI的熔点沸点升高与范德华力大小有关 |
B、CO的一种等电子体为NO+,它的电子式为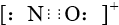 |
| C、H2O的熔点沸点大于H2S,是由于H2O分子之间存在氢键这种化学键 |
| D、电子层序数越大,s原子轨道的形状相同、半径越大 |
考点:同一主族内元素性质递变规律与原子结构的关系,原子核外电子排布,“等电子原理”的应用,氢键的存在对物质性质的影响
专题:
分析:A.氢化物的相对分子质量越大,分子间的范德华力越大,沸点越高;
B.等电子体的结构相似;
C.氢键不属于化学键;
D.s原子轨道为球形.
B.等电子体的结构相似;
C.氢键不属于化学键;
D.s原子轨道为球形.
解答:
解:A.氢化物的相对分子质量越大,分子间的范德华力越大,沸点越高,则从HCl、HBr到HI的熔点沸点升高与范德华力大小有关,故A正确;
B.等电子体的结构相似,CO的一种等电子体为NO+,则它们的结构相似,原子间都含有三键,即含有三个共用电子对,则它的电子式为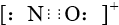 ,故B正确;
,故B正确;
C.H2O的熔点沸点大于H2S,是由于H2O分子之间存在氢键,氢键属于分子间作用力,不属于化学键,故C错误;
D.s原子轨道为球形,电子层序数越大,原子轨道距离原子核越远,原子轨道的半径越大,故D正确.
故选C.
B.等电子体的结构相似,CO的一种等电子体为NO+,则它们的结构相似,原子间都含有三键,即含有三个共用电子对,则它的电子式为
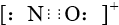 ,故B正确;
,故B正确;C.H2O的熔点沸点大于H2S,是由于H2O分子之间存在氢键,氢键属于分子间作用力,不属于化学键,故C错误;
D.s原子轨道为球形,电子层序数越大,原子轨道距离原子核越远,原子轨道的半径越大,故D正确.
故选C.
点评:本题考查了分子间作用力、氢键、电子式、原子轨道,题目涉及的知识点较多,侧重于基础知识的应用的考查,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、小苏打是弱电解质,其水溶液导电能力很弱 |
| B、氨气是非电解质,但氨水能导电 |
| C、稀释醋酸溶液,可以促进醋酸分子电离使溶液pH减小 |
| D、硫酸是强电解质,在水溶液和熔融状态下均能导电 |
下列家庭小实验不能制得溶液的是( )
A、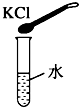 |
B、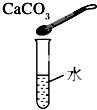 |
C、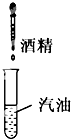 |
D、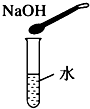 |
关于Cl-的说法正确的是( )
| A、Cl-呈黄绿色 |
| B、Cl-有毒 |
| C、Cl-具有17个电子 |
| D、Cl-是稳定结构 |
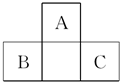 如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答:
如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答: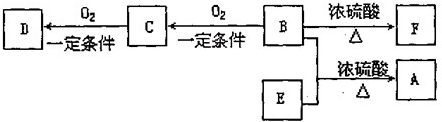
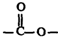 基团.
基团.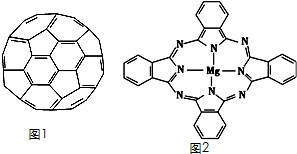
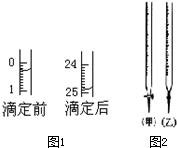 某研究性学习小组的同学用标准浓度的烧碱溶液测定未知浓度的盐酸.
某研究性学习小组的同学用标准浓度的烧碱溶液测定未知浓度的盐酸.