题目内容
16.下列各组有机物只用一种试剂无法鉴别的是( )| A. | 乙醇、戊烷、硝基苯 | B. | 苯、四氯化碳、己烯 | ||
| C. | 苯、甲苯、环己烷 | D. | 甲醇、乙酸乙酯、乙酸 |
分析 A.乙醇与水混溶,戊烷、硝基苯不溶于水,但密度不同;
B.己烯使溴水褪色,苯、四氯化碳与溴水会分层,但是密度不同;
C.苯、甲苯、环己烷性质稳定,不溶于水;
D.甲醇与饱和碳酸钠溶液互溶,乙酸乙酯难溶于碳酸钠溶液,乙酸与碳酸钠反应生成气体.
解答 解:A.乙醇与水混溶,戊烷、硝基苯不溶于水,戊烷的密度比水小,硝基苯的密度比水大,可用水鉴别,故A不选;
B.己烯使溴水褪色,苯、四氯化碳与溴水会分层,但是密度不同,所以可以用溴水鉴别,故B不选;
C.苯、甲苯、环己烷性质稳定,不溶于水,只用一种试剂无法鉴别,故C选;
D.甲醇与饱和碳酸钠溶液互溶,乙酸乙酯难溶于碳酸钠溶液,乙酸与碳酸钠反应生成气体,所以可加饱和碳酸钠溶液鉴别,故D不选.
故选C.
点评 本题考查有机物的鉴别,题目难度不大,注意把握有机物性质的异同,为解答该题的关键点,学习中要注重相关基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.CuSO4溶液中加入过量KI溶液,产生白色CuI沉淀,溶液变棕色.向反应后溶液中通入过量SO2,溶液变成无色.下列说法错误的是( )
| A. | 滴加KI溶液时,KI被氧化,CuI是还原产物 | |
| B. | 通入SO2后,溶液变无色,体现SO2的还原性 | |
| C. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 | |
| D. | 整个过程发生了复分解反应和氧化还原反应 |
11.实验室用大理石和盐酸制备CO2,下列措施可使反应速率加快的是( )
| A. | 降低反应温度 | B. | 延长反应时间 | C. | 粉碎大理石 | D. | 加水稀释盐酸 |
1.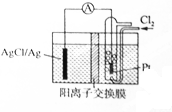 某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl,电解液为1mol•L-1的盐酸.下列说法正确的是( )
某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl,电解液为1mol•L-1的盐酸.下列说法正确的是( )
 某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl,电解液为1mol•L-1的盐酸.下列说法正确的是( )
某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl,电解液为1mol•L-1的盐酸.下列说法正确的是( )| A. | 正极反应为AgCl+e-═Ag+Cl- | |
| B. | 放电时交换膜右侧溶液中有大量白色沉淀生成 | |
| C. | 放电后交换膜溶液酸性增强 | |
| D. | 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02mol离子 |
8.下列说法不正确的是( )
| A. | 新制氯水中存在两种电离平衡 | |
| B. | 不同原子之间形成的共价键不一定是极性共价键 | |
| C. | 向久置于空气中的Na2SiO3、NaOH、CaCl2、漂白粉溶液里加足量盐酸,都能产生气体 | |
| D. | 将少量酸化的FeCl2溶液滴入过氧化氢溶液中,溶液变黄,并产生大量的气泡. |
6.可逆反应N2+3H2?2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示.下列关系中能说明反应已达到平衡状态的是( )
| A. | v正(N2)=3v逆(H2) | B. | v正(N2)=3v正(H2) | C. | 2v正(H2)=3 v逆(NH3) | D. | v正(N2)=v逆(NH3) |
 .
.