题目内容
1.海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在.有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘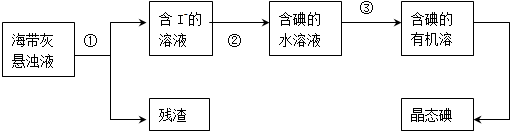
(1)灼烧海带时需要用到的实验仪器是CDEF (从下列仪器中选出所需 的仪器,用标号字母填写在空白处).
A.烧杯 B.蒸发皿 C.坩埚 D.三角架 E.酒精灯 F.泥三角
(2)指出上图中提取碘的过程中有关的实验操作名称:①过滤,③萃取、分液.
(3)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50ml碘水和15ml四氯化碳溶液加入分液漏斗中,并盖好玻璃塞;
C.检查分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层.
(a)过程③正确操作步骤的顺序是:(填编号字母)CBDAHGEF;
(b)上述G步操作的目的是:使分液漏斗内外空气相通,以保证液体能顺利流出;
(c) 最后碘的有机溶液是通过漏斗下口获得(填“漏斗上口”或“漏斗下口”).
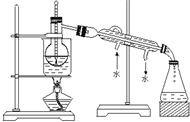
(4)从含碘的有机溶液中提取碘和回收有机试剂,还需要经过蒸馏,观察下图所示实验装置指出其错误缺石棉网;温度计的位置应将水银球置于蒸馏烧瓶支管口处,冷凝水应下进上出;尾接管与锥形瓶之间不应有塞子.
分析 以海带为原料获得少量碘单质:将海带在坩埚中灼烧得到海带灰,将海带灰浸泡得到海带灰悬浊液,然后采用过滤的方法将残渣和溶液分离,得到含有碘化钾的溶液,向水溶液中通入足量Cl2,发生反应为2I-+Cl2=2Cl-+I2,向含有碘单质的溶液中加入萃取剂四氯化碳萃取蒸馏得到碘单质.
(1)根据仪器的作用选取仪器;
(2)分离不溶性固体和溶液采用过滤的方法,从碘水中获得碘采用萃取的方法;
(3)(a)其实验步骤是检漏、加药品、振荡、放置、静置、打开玻璃塞、旋开活塞、倒出液体;
(b)分液漏斗使用时:将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准,平衡气压;
(c)密度大于水的萃取剂从下口流出,密度小于水的从上口倒出;
(4)从含碘的有机溶液中提取碘和回收有机试剂,还需要经过蒸馏,对照蒸馏操作,如图2错误为缺少石棉网,温度计水银球位置错误,冷凝水水流方向错误,尾接管与锥形瓶之间不应有塞子.
解答 解:(1)灼烧海带时用坩埚盛放海带,用带铁圈的铁架台或三脚架和泥三角上放置坩埚,用酒精灯进行加热,所以灼烧海带时需要用到的实验仪器是坩埚、带铁圈的铁架台或三脚架、泥三角、酒精灯;
故答案为:CDEF;
(2)将溶液和不溶性固体分离的方法是过滤,从碘水中获取碘单质采用萃取、分液的方法,
故答案为:过滤;萃取、分液;
(3)(a)其实验步骤是检漏、加药品、振荡、放置、静置、打开玻璃塞、旋开活塞、倒出液体,所以其操作顺序是CBDAHGEF,
故答案为:CBDAHGEF;
(b)分液漏斗使用时:将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准,可以平衡气压,便于液体流出,
故答案为:使分液漏斗内外空气相通,以保证液体能顺利流出;
(c)分液漏斗中的下层液体从下口漏出,上层液体从上口倒出,萃取剂四氯化碳的密度大于水,含有碘单质的四氯化碳在下层,从下口漏出,选用苯/汽油/煤油这些物质密度小于水,应从漏斗上口倒出,
故答案为:漏斗下口;
(4)由图可知,烧瓶底部表面积大,加热需要石棉网使其受热均匀,温度计水银球应与烧瓶支管口相平测蒸汽温度,冷却水应下进上出与热气体对流,尾接管与锥形瓶之间不应有塞子,不便于液体流出,
故答案为:缺石棉网;温度计的位置应将水银球置于蒸馏烧瓶支管口处,冷凝水应下进上出;尾接管与锥形瓶之间不应有塞子.
点评 本题考查了海水资源的分析应用,实验设计和过程分析,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力,题目难度中等.

(1)Cu+2Ag+→Cu2++2Ag;(2)Fe+Cu2+→Fe2++Cu.
根据上述反应,判断Ag+、Cu2+、Fe2+氧化性强弱顺序排列正确的是( )
| A. | Ag+>Cu2+>Fe2+ | B. | Cu2+>Ag+>Fe2+ | C. | Ag+>Fe2+>Cu2+ | D. | Fe2+>Cu2+>Ag+ |
| A. | 加热分解NH4HCO3 | B. | 加热NaHCO3 | C. | 熔化烧碱 | D. | 加热NaCl |
| A. | CH4与P4的分子结构都是正四面体形,因此在NA个CH4分子或P4分子中都含有4NA个共价键 | |
| B. | 在含NA个硅原子的二氧化硅晶体中含有4NA个Si-O键 | |
| C. | 5.6 g Fe与含0.2 mol HNO3的溶液充分反应,至少失去0.2NA个电子 | |
| D. | NA个Fe3+完全水解可以得到NA个氢氧化铁胶体粒子 |
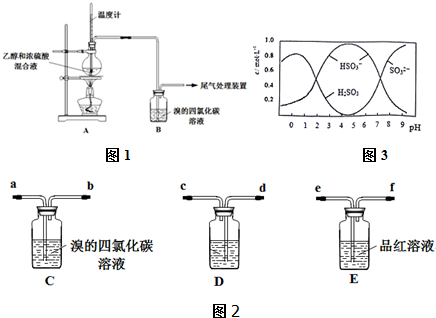
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=═CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略如图1).
实验操作和现象:
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,使B中溶液褪色反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br;
②乙根据现象认为实验中产生的SO2和H2O,使B中有色物质反应褪色.
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色.
乙:用下列装置按一定顺序与A连接:(尾气处理装置略如图2)
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色.
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是NaOH溶液;乙设计的实验D中盛放的试剂是浓硫酸,装置连接顺序为(d)cabe(f).
b.能说明确实是SO2使E中溶液褪色的实验是加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2.
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂.
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图3所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol•L-1],此时溶液中c(SO32-)≤0.05mol•L-1.
| A. | 可用了达尔现象区分溶液与胶体 | |
| B. | 生石灰与水混合的过程只发生物理变化 | |
| C. | 明矾净水只发生了物理变化 | |
| D. | CuSO4•5H20 是一种混合物 |
