题目内容
19.下列有关实验的说法正确的是( )| A. | 配制FeSO4溶液,应先将盐溶解在稀硫酸中,再加水稀释到所需浓度,并加入少量铁屑 | |
| B. | 切割白磷时,必须用镊子夹取,置于桌面上的玻璃片上,小心用刀切割 | |
| C. | 向淀粉溶液中加入稀硫酸,水浴加热一段时间.要证明淀粉已水解,取样后加入银氨溶液,水浴加热,观察是否有银镜生成 | |
| D. | 配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
分析 A.Fe2+容易被氧化;
B.白磷容易自燃;
C.银镜反应应在碱性条件下进行;
D.量筒不能用于配制溶液.
解答 解:A.因为亚铁离子在空气中极易被氧化成三价铁离子所以要求有过量铁屑可以和三价铁离子反应生成亚铁离子Fe+Fe3+=2Fe2+,故A正确;
B.因白磷容易自燃,在水中切割,故B错误;
C.银镜反应应在碱性条件下进行,应先加入碱调节溶液至碱性,否则不能生成银镜,故C错误;
D.量筒不能用于配制溶液,应改为烧杯中进行,故D错误.
故选A.
点评 本题考查较为综合,涉及溶液配制、银镜反应以及实验操作等知识,为高频考点,侧重于基础知识的综合理解与运用的考查,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 1.0 mol•L-1的KNO3溶液中:H+、Fe2+、Cl-、SO42- | |
| B. | c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- | |
| C. | 能使pH试纸变红的溶液中:K+、Ba2+、AlO2-、Cl- | |
| D. | pH=0的溶液中:Mg2+、Na+、F-、SO42- |
7.下列有关实验的描述正确的是( )
| 选项 | 操作 | 实验目的 |
| A | 沿玻璃棒将蒸馏水缓慢倒入盛有浓硫酸的烧杯中,边加边搅拌 | 稀释浓硫酸 |
| B | 测定相同浓度的Na2SO4和Na2SiO3溶液的pH值 | 比较硫和硅的非金属性强弱 |
| C | 将铁的氧化物溶于过量稀盐酸中,再滴加几滴紫红色KMnO4溶液 | 判断某铁的氧化物是否含有Fe2+ |
| D | 用装有双氧水的碱式滴定管,采用淀粉溶液作为指示剂,滴定NaCl和NaI混合溶液 | 测定NaI的含量 |
| A. | A | B. | B | C. | C | D. | D |
14.下列装置及操作能达到实验目的是( )
| A. | 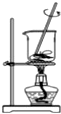 蒸发食盐水得到氯化钠晶体 | B. | 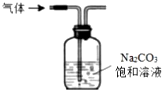 除去CO2中含有少量HCl气体 | ||
| C. | 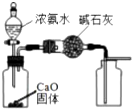 制取并收集干燥纯净的NH3 | D. |  验证SO2的还原性 |
4.含有5个碳原子的饱和一元醇C5H12O的同分异构体中,能被气体成醛的有( )
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
11.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.工业上先制得高铁酸钠,然后在低温下,在高铁酸铁的溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4).
湿法制备:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,
干法制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法错误的是( )
湿法制备:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,
干法制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法错误的是( )
| A. | 干法中生成的高铁酸钠既是氧化产物又是还原产物 | |
| B. | 湿法中每生成1mol Na2FeO4 转移3mol电子 | |
| C. | 干法中每生成1 mol Na2FeO4 转移4mol电子 | |
| D. | K2FeO4处理水时,不仅能消毒杀菌,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质 |
8.下列反应的离子方程式书写正确的是( )
| A. | MgO溶于稀盐酸中:O2-+2H+═H2O | |
| B. | 碳酸钙中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 实验室用MnO2反应制Cl2:MnO2+2H++2Cl-═Cl2↑+Mn2++H2O | |
| D. | 向氢氧化钠溶液中通入过量二氧化碳:OH-+CO2=HCO3- |
9.现有如下反应热信息
下列说法正确的是( )
| 热化学方程式 | △H |
| 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(1) | -2600 kJ•mol-1 |
| 2C6H6(g)+15O2(g)═12CO2(g)+6H2O(1) | -6590 kJ•mol-1 |
| 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(g) | -a kJ•mol-1 |
| 2C6H6(1)+15O2(g)═12CO2(g)+6H2O(1) | -b kJ•mol-1 |
| A. | a>2600 | |
| B. | b>6590 | |
| C. | 相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C2H2(g)放热更多 | |
| D. | C2H2(g)三聚生成C6H6(g)的过程属于吸热反应 |