题目内容
13.某强酸性溶液中可能存在NO3-、I-、Cl-、Fe3+中的一种或几种.向该溶液加入溴水后,溴被还原,由此推断该溶液中( )| A. | 不含NO3-,也不含Fe3+ | B. | 含有NO3-、I-、Cl- | ||
| C. | 含I-,不含Cl- | D. | 含有Fe3+ |
分析 溶液呈强酸性,向该溶液中滴入Br2,单质Br2被还原,说明溶液中含有还原性离子,为I-,则氧化性离子不能存在,以此来解答.
解答 解:溶液呈强酸性,
向该溶液中滴入Br2,单质Br2被还原,说明溶液中含有还原性离子,可知一定含I-,
因NO3-、Fe3+具有强氧化性,与I-发生氧化还原反应而不能大量共存,
由于Cl-不发生反应,不能确定是否含有Cl-,
故选A.
点评 本题考查常见离子的检验及离子共存,为高考常见题型和高频考点,侧重于学生的分析能力和应用能力的考查,注意把握氧化还原反应的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列装置或操作能达到实验目的是( )
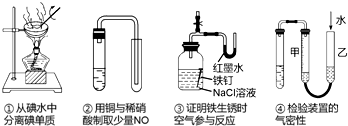

| A. | ①③ | B. | ②④ | C. | ③④ | D. | ①②③④ |
1.下列说法中正确的是(设NA表示阿伏加德罗常数)( )
| A. | NA个氮气分子与NA个一氧化碳分子所含的电子数相等 | |
| B. | 在标准状况下,1摩尔铜恰好与400ml 10mol/L的浓硝酸反应,可收集到22.4L的气体 | |
| C. | 2mol•L-1 氨水溶液中含有2NA个NH4+ | |
| D. | 1mol氨气溶于1升水中,所得溶液的浓度为1mol/L |
8.X、Y、Z三种气体都能污染大气,由于它们都能与碱反应,因此,在工业上常用碱液来吸收它们.其中,X是活泼非金属元素的单质,工业上制造漂白粉时要用到它;Y是煤燃烧的产物之一,是形成酸雨的主要物质;Z为汽车尾气中的有害物质之一,是一种红棕色气体.
(1)写出这三种气体的化学式:XCl2、YSO2、ZNO2.
(2)分别写出他们与水反应的化学方程式,指出这些反应中哪些是氧化还原反应.
(1)写出这三种气体的化学式:XCl2、YSO2、ZNO2.
(2)分别写出他们与水反应的化学方程式,指出这些反应中哪些是氧化还原反应.
| 气体和水反应的化学方程式 | 是否氧化还原反应 (填“是”或“否”) | |
| X+H2O | ||
| Y+H2O | ||
| Z+H2O |
18.近期我国冀东渤海湾发现储量达10亿吨的大型油田.下列关于石油的说法正确的是( )
| A. | 石油主要含有碳、氢两种元素 | B. | 石油属于可再生矿物能源 | ||
| C. | 石油的裂化是化学变化 | D. | 石油分馏的各馏分均是纯净物 |
5.化学能与热能、电能等能相互转化.关于化学能与其他能量相互转化的说法正确的是( )
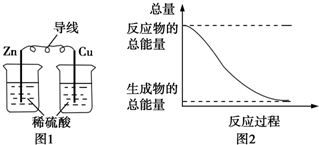

| A. | 图1所示的装置能将化学能转变为电能 | |
| B. | 图2所示的反应为吸热反应 | |
| C. | 中和反应中,反应物的总能量比生成物的总能量低 | |
| D. | 化学反应中能量变化的主要原因是化学键的断裂与生成 |
2.五种短周期主族元素X、Y、Z、W、R,X的原子半径是短周期主族元素中最大的,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m一n,W元素与Z元素同主族,R元素与Y元素同主族.下列叙述错误的是( )
| A. | 60 g ZY2中含有2 mol Z-Y极性共价键 | |
| B. | Y的氢化物比R的氢化物稳定,熔沸点高 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z | |
| D. | X与Y形成的两种常见化合物中阴、阳离子的个数比均为1:2 |
3.X、Y、Z、W是原子序数依次增大的短周期元素,Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4,下列说法正确的是( )
| A. | 原子半径:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y的简单气态氢化物的热稳定性比Z的强 | |
| C. | 由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应 | |
| D. | 由X、Y、Z三种元素组成的化合物可以是酸、碱或盐 |