题目内容
关于 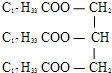 ,下列说法正确的是( )
,下列说法正确的是( )
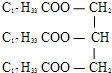 ,下列说法正确的是( )
,下列说法正确的是( )| A、属于油脂,名为硬脂酸甘油酯 |
| B、常温下呈固态 |
| C、属于高分子化合物 |
| D、碱性条件下能发生皂化反应 |
考点:油脂的性质、组成与结构
专题:
分析:A.该油脂属于油酸甘油酯;
B.油酸甘油酯常温下为液态;
C.油脂不是高分子化合物;
D.油脂在碱性条件下的水解反应为皂化反应.
B.油酸甘油酯常温下为液态;
C.油脂不是高分子化合物;
D.油脂在碱性条件下的水解反应为皂化反应.
解答:
解:A.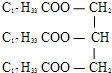 中烃基属于不饱和烃基,则该油脂属于油酸甘油酯,故A错误;
中烃基属于不饱和烃基,则该油脂属于油酸甘油酯,故A错误;
B.油酸甘油酯常温下为液态,不是固态,硬脂酸甘油酯常温下呈固态,故B错误;
C.油脂不是高分子化合物,分子量在一万以上的化合物属于高分子化合物,故C错误;
D.油脂在碱性条件下的水解反应为皂化反应,则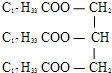 碱性条件下能发生皂化反应,故D正确.
碱性条件下能发生皂化反应,故D正确.
故选D.
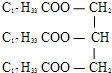 中烃基属于不饱和烃基,则该油脂属于油酸甘油酯,故A错误;
中烃基属于不饱和烃基,则该油脂属于油酸甘油酯,故A错误;B.油酸甘油酯常温下为液态,不是固态,硬脂酸甘油酯常温下呈固态,故B错误;
C.油脂不是高分子化合物,分子量在一万以上的化合物属于高分子化合物,故C错误;
D.油脂在碱性条件下的水解反应为皂化反应,则
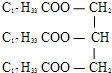 碱性条件下能发生皂化反应,故D正确.
碱性条件下能发生皂化反应,故D正确.故选D.
点评:本题考查了油脂的结构和性质,注意油脂的组成和结构,特别是硬脂酸甘油酯、软脂酸甘油酯和油酸甘油酯的区别,题目难度不大.

练习册系列答案
相关题目
汽车的启动电源常用铅蓄电池,电池反应如下:PbO2+Pb+2H2SO4
2PbSO4+2H2O,根据此反应判断下列叙述中正确的是( )
| 放电 |
| 充电 |
| A、电池放电时,PbO2是负极;充电时,PbO2是电池的阳极 |
| B、负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C、放电时,PbO2得电子,被氧化 |
| D、电池放电时,溶液酸性增强 |
在NaCl、MgSO4、MgCl2和三种盐配成的混合溶液中,若Na+的浓度为0.1mol/L、Mg2+的浓度为0.25mol/L、Cl-的浓度为0.2mol/L,则SO42-的物质的量浓度为( )
| A、0.5mol?L-1 |
| B、0.45mol?L-1 |
| C、0.2mol?L-1 |
| D、0.25mol?L-1 |
下列实验设计及其对应的离子方程式均正确的是( )
| A、醋酸溶液除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B、氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| C、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| D、向AlCl3溶液中通入过量NH3:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
下列分子式表示的物质,具有同分异构体的是( )
| A、C6H6 |
| B、C3H8 |
| C、CH2Cl2 |
| D、CH2O |
把一定量的NaHCO3和Na2O2的混合物放在密闭容器中加热.关于混合物加热前后消耗盐酸的物质的量,下列结论判断正确的是( )
| A、加热前消耗的多 |
| B、加热前加热后消耗的一样多 |
| C、加热后消耗的多 |
| D、无法确定 |
某溶液灼烧时,透过蓝色钴玻璃看到紫色火焰,下列判断中错误的是( )
| A、该溶液中不可能含钾单质 |
| B、该溶液中不可能含钠的化合物 |
| C、该溶液中一定含钾元素 |
| D、该溶液中可能含钠的化合物 |
等质量的C72和C60,下列说法正确的是( )
| A、物质的量相等 |
| B、分子个数相等 |
| C、原子个数相等 |
| D、以上说法都不正确 |