题目内容
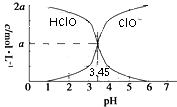 25℃时,2a mol?L-1次氯酸水溶液中,用NaOH溶液调节其pH(忽略溶液体积的变化),得到c(HClO)、c(ClO-)与溶液pH的变化关系如图所示.下列说法正确的是( )
25℃时,2a mol?L-1次氯酸水溶液中,用NaOH溶液调节其pH(忽略溶液体积的变化),得到c(HClO)、c(ClO-)与溶液pH的变化关系如图所示.下列说法正确的是( )| A、当pH=2时,溶液中c(ClO-)>c(Na+) |
| B、当c(ClO-)>c(HClO)时,溶液一定呈碱性 |
| C、当pH=3.45时,所加NaOH溶液恰好与HClO完全反应 |
| D、当pH=5时,溶液中:c(HClO)+c(Na+)+c(H+)-c(OH-)=2a mol?L-1 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.pH=2时,溶液显示酸性,则c(OH-)<c(H+),根据电荷守恒判断c(ClO-)、c(Na+)的大小;
B.根据图象可知,当pH>3.45时,溶液中c(ClO-)>c(HClO),据此进行判断;
C.当次氯酸与氢氧化钠恰好反应时生成次氯酸钠溶液,溶液显示碱性,而pH=3.4时显示酸性;
D.根据混合液中电荷守恒、物料守恒进行解答.
B.根据图象可知,当pH>3.45时,溶液中c(ClO-)>c(HClO),据此进行判断;
C.当次氯酸与氢氧化钠恰好反应时生成次氯酸钠溶液,溶液显示碱性,而pH=3.4时显示酸性;
D.根据混合液中电荷守恒、物料守恒进行解答.
解答:
解:A.当pH=2,溶液呈酸性,则溶液中c(OH-)<c(H+),溶液中存在电荷守恒c(Na+)+c(H+)=c(OH-)+c(ClO-),则c(ClO-)>c(Na+),故A正确;
B.根据图象知,当pH>3.45时,溶液中c(ClO-)>c(HClO),所以当c(ClO-)>c(HClO)时,溶液不一定成碱性,故B错误;
C.HClO为弱酸,恰好反应时生成次氯酸钠溶液,溶液显示碱性,而当pH=3.45时溶液显示酸性,则HClO酸过量,故C错误;
D.溶液中都存在电荷守恒:①c(Na+)+c(H+)=c(OH-)+c(ClO-),根据物料守恒得:②c(HClO)+c(ClO-)=2amol/L,当pH=5时,由①可得:③c(Na+)+c(H+)-c(OH-)=c(ClO-),③两边同时加c(HClO)可得:c(HClO)+c(Na+)+c(H+)-c(OH-)=c(HClO)+c(ClO-)=2a mol?L-1,故D正确;
故选AD.
B.根据图象知,当pH>3.45时,溶液中c(ClO-)>c(HClO),所以当c(ClO-)>c(HClO)时,溶液不一定成碱性,故B错误;
C.HClO为弱酸,恰好反应时生成次氯酸钠溶液,溶液显示碱性,而当pH=3.45时溶液显示酸性,则HClO酸过量,故C错误;
D.溶液中都存在电荷守恒:①c(Na+)+c(H+)=c(OH-)+c(ClO-),根据物料守恒得:②c(HClO)+c(ClO-)=2amol/L,当pH=5时,由①可得:③c(Na+)+c(H+)-c(OH-)=c(ClO-),③两边同时加c(HClO)可得:c(HClO)+c(Na+)+c(H+)-c(OH-)=c(HClO)+c(ClO-)=2a mol?L-1,故D正确;
故选AD.
点评:本题考查了离子浓度大小的判断,明确图象中pH与微粒大小的关系即可解答,结合物料守恒和电荷守恒分析,题目难度中等,易错选项是B,当c(ClO-)>c(HClO),溶液不一定呈碱性,可能为酸性或中性,为易错点.

练习册系列答案
相关题目
下列对于“摩尔”的理解正确的是( )
| A、摩尔是国际科学界建议采用的一种物理量 |
| B、摩尔是物质的量的单位,简称摩,符号为mol |
| C、摩尔可以把物质的宏观质量与微观粒子的数量联系起来 |
| D、国际上规定,0.012 kg12C所含有的碳原子的物质的量为1 mol |
对于胃溃疡较重的病人,不适合使用的抑酸剂是( )
| A、氢氧化镁 |
| B、氢氧化铝 |
| C、碳酸氢钠 |
| D、Na3C6H5O7﹒2H2O |
用10ml 0.1mol/L的AgNO3溶液恰好与相同体积的NaCl、MgCl2和AlCl3三种溶液完全反应,则这三种盐酸盐溶液的物质的量浓度之比是( )
| A、3:2:2 |
| B、6:3:2 |
| C、1:3:3 |
| D、3:1:1 |
下列有关物质分类或归类正确的是( )
①混合物:漂白粉、水玻璃、Fe(OH)3胶体、水银
②化合物:CaCl2、NaOH、HCl、HD
③电解质:胆矾、苛性钾、冰醋酸、氧化钠
④同素异形体:C60、碳纳米管、金刚石、石墨
⑤硅酸盐:光导纤维、水晶、玻璃、水玻璃
⑥煤的干馏、煤的汽化和液化都属于化学变化.
①混合物:漂白粉、水玻璃、Fe(OH)3胶体、水银
②化合物:CaCl2、NaOH、HCl、HD
③电解质:胆矾、苛性钾、冰醋酸、氧化钠
④同素异形体:C60、碳纳米管、金刚石、石墨
⑤硅酸盐:光导纤维、水晶、玻璃、水玻璃
⑥煤的干馏、煤的汽化和液化都属于化学变化.
| A、③④⑥ | B、②③⑥ |
| C、①②③④⑥ | D、①②④⑤ |
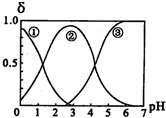 在H2C2O4(草酸)水溶液中,H2C2O4、HC2O4-和C2O42-三种形态的炷子的分布分数δ随溶液pH变化的关系如图所示[已知KSP(CaC2O4)=2.3×10-9].下列说法正确的是( )
在H2C2O4(草酸)水溶液中,H2C2O4、HC2O4-和C2O42-三种形态的炷子的分布分数δ随溶液pH变化的关系如图所示[已知KSP(CaC2O4)=2.3×10-9].下列说法正确的是( )| A、曲线①代表的粒子是HC2O4- |
| B、pH=5时,溶液中:c(C2O42-)>c(H2C2O4)>c(HC2O4-) |
| C、0.1mol?L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) |
| D、一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)减小,c(Ca2+)不变 |
化学无处不在,运用化学知识判断下列与化学有关的说法正确的是( )
| A、地沟油的主要成分是高级脂肪酸甘油酯,可用于制肥皂和加工食用油 |
| B、SO2能漂白纸浆等,故可广泛用于食品的漂白 |
| C、高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害 |
| D、为防止富脂食品氧化变质,常在包装袋中放入生石灰 |
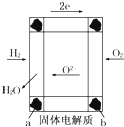 据报道,科学家已经研制出固体氧化物燃料电池,该电池以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,其工作原理如图所示(多孔电极a、b均不参加电极反应).下列说法正确的是( )
据报道,科学家已经研制出固体氧化物燃料电池,该电池以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,其工作原理如图所示(多孔电极a、b均不参加电极反应).下列说法正确的是( )| A、有H2O放出的a极为电池的正极 |
| B、b极对应的电极反应式为:O2+4e-+2H2O-→4OH- |
| C、正极对应的电极反应式为:O2+4H++4e--→2H2O |
| D、该电池的总反应式为:2H2+O2═2H2O |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、常温常压下,11.2L氧气含有的原子数目为NA |
| B、14gN2和N4组成的混合气体中含有的原子数为NA |
| C、0.1NA个二氧化碳分子所占体积约为2.24L |
| D、1mol/L CaCl2溶液中含有的氯离子数目为2NA |