题目内容
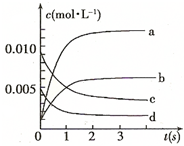 (14分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
(14分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(N O)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
K300°C>K350°C,则该反应是
(2)如图中表示NO2的变化的曲线是
(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.NO、O2、NO2的浓度之比为2:1:2
d.容器内密度保持不变
e.容器内气体的颜色不再变化
(4)缩小容器体积使压强增大,平衡向
考点:化学平衡常数的含义,化学平衡的影响因素,化学平衡状态的判断,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)依据化学方程式结合平衡常数概念书写平衡常数表达式;平衡常数越大说明平衡正向进行程度越大;
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO);根据v=
计算v(NO),再利用速率之比等于化学计量数之比计算v(O2);
(3)可逆反应达到平衡时,v正=V逆 (同种物质表示)或正逆速率之比等于化学计量数之比(不同物质表示),反应混合物各组分的物质的量、浓度、含量不再变化,以及由此衍生的一些量也不发生变化,由此进行判断.
(4)反应前后气体体积减小缩小容器体积使压强增大,平衡正向进行,平衡常数随温度变化,不随压强变化.
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO);根据v=
| △c |
| △t |
(3)可逆反应达到平衡时,v正=V逆 (同种物质表示)或正逆速率之比等于化学计量数之比(不同物质表示),反应混合物各组分的物质的量、浓度、含量不再变化,以及由此衍生的一些量也不发生变化,由此进行判断.
(4)反应前后气体体积减小缩小容器体积使压强增大,平衡正向进行,平衡常数随温度变化,不随压强变化.
解答:
解:(1)2NO(g)+O2(g)═2NO2(g),依据化学方程式写出平衡常数表达式为:
;
故答案为:
;K300°C>K350°C,说明温度越高平衡常数越小,平衡逆向进行,逆向是吸热反应,正向是放热反应,则该反应是放热反应;
故答案为:
;放;
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO)=
=0.0065mol/L,所以图中表示NO2变化的曲线是b,
故答案为:b;
2s内用NO表示的平均反应速率v(NO)=
=
=3.0×10-3mol?L-1?s-1,速率之比等于化学计量数之比,
所以v(O2)=
v(NO)=
×3.0×10-3mol?L-1?s-1=1.5×10-3mol?L-1?s-1,故答案为:1.5×10-3mol?L-1?s-1;
(3)2NO(g)+O2(g)═2NO2(g),反应是气体体积减小的放热反应
a、v(NO2)=2v(O2) 表示同一方向反应速率,v(NO2)自始至终为v(O2)的2倍,不能说明达到平衡,故a错误;
b、随反应进行,反应混合气体总的物质的量在减小,压强之比等于气体物质的量之比,气体压强保持不变,说明反应到达平衡,故b正确;
c、平衡浓度和起始量和转化率有关,NO、O2、NO2的浓度之比为2:1:2,不能说明反应达到平衡状态,故c错误;
d、反应前后气体质量守恒,体积不变,反应过程中和平衡状态下,气体密度都不变,所以不能说明反应达到平衡状态,故d错误;
e、反应中二氧化氮气体是红棕色气体,容器内气体的颜色不再变化,说明二氧化氮气体浓度不变,说明反应达到平衡状态,故e正确;
故答案为:be;
(4)反应前后气体体积减小缩小容器体积使压强增大,平衡正向进行,平衡常数随温度变化,不随压强变化;
故答案为:正;不变.
| c2(NO2) |
| c2(NO)c(O2) |
故答案为:
| c2(NO2) |
| c2(NO)c(O2) |
故答案为:
| c2(NO2) |
| c2(NO)c(O2) |
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO)=
| 0.020mol-0.007mol |
| 2L |
故答案为:b;
2s内用NO表示的平均反应速率v(NO)=
| ||
| △t |
| ||
| 2s |
所以v(O2)=
| 1 |
| 2 |
| 1 |
| 2 |
(3)2NO(g)+O2(g)═2NO2(g),反应是气体体积减小的放热反应
a、v(NO2)=2v(O2) 表示同一方向反应速率,v(NO2)自始至终为v(O2)的2倍,不能说明达到平衡,故a错误;
b、随反应进行,反应混合气体总的物质的量在减小,压强之比等于气体物质的量之比,气体压强保持不变,说明反应到达平衡,故b正确;
c、平衡浓度和起始量和转化率有关,NO、O2、NO2的浓度之比为2:1:2,不能说明反应达到平衡状态,故c错误;
d、反应前后气体质量守恒,体积不变,反应过程中和平衡状态下,气体密度都不变,所以不能说明反应达到平衡状态,故d错误;
e、反应中二氧化氮气体是红棕色气体,容器内气体的颜色不再变化,说明二氧化氮气体浓度不变,说明反应达到平衡状态,故e正确;
故答案为:be;
(4)反应前后气体体积减小缩小容器体积使压强增大,平衡正向进行,平衡常数随温度变化,不随压强变化;
故答案为:正;不变.
点评:本题考查了化学平衡影响因素、平衡标志分析判断,平衡常数、反应速率的计算应用,掌握基础和移动原理是关键,题目难度中等.

练习册系列答案
相关题目
最近,意大利科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子O4,并用质谱仪探测到了它存在的证据.下列说法正确的是( )
| A、O4是氧元素的一种同位素 |
| B、O4可能含有极性键 |
| C、同温同压下,等体积的O4气体和O2含有相同的分子数 |
| D、O4转化O2为物理变化 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O═CH3COOH+4H+.下列有关说法正确的是( )
| A、正极上发生的反应是:O2+4e-+2H2O═4OH- | ||||
B、该电池反应的化学方程式为:CH3CH2OH+3O2
| ||||
| C、检测时,电解质溶液中的H+向正极移动 | ||||
| D、若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
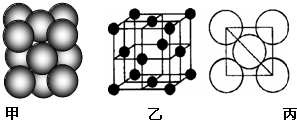
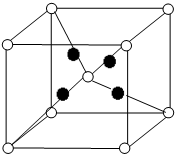 X、Y、Z、W为短周期的主族元素,其原子序数依次增大.X元素形成的单质是自然界中含量最多的气体.Y是电负性最大的元素.W的原子最外层电子数与核外电子总数之比为3:8.X的原子序数是Z的原子序数的一半.U原子基态的外围电子排布3d104s1.
X、Y、Z、W为短周期的主族元素,其原子序数依次增大.X元素形成的单质是自然界中含量最多的气体.Y是电负性最大的元素.W的原子最外层电子数与核外电子总数之比为3:8.X的原子序数是Z的原子序数的一半.U原子基态的外围电子排布3d104s1.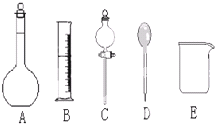 我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL 0.1mol?L-1的盐酸溶液.
我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL 0.1mol?L-1的盐酸溶液.