题目内容
13.常温下,有下列四种溶液:下列说法正确的是( )| ① | ② | ③ | ④ |
| 0.1mol/LNaOH溶液 | pH=11NaOH溶液 | 0.1mol/L CH3COOH溶液 | pH=3CH3COOH溶液 |
| A. | 由水电离出H+的浓度c(H+):①>③ | |
| B. | 将④加蒸馏水稀释至原来的100倍时,所得溶液的PH>5 | |
| C. | ①与③混合,若溶液pH=7,则体积:V(NaOH)>V(CH3COOH) | |
| D. | 等体积等PH的④溶液和盐酸分别与足量的Zn反应,④溶液生成同条件下氢气体积多 |
分析 A.酸碱溶液都抑制了水的电离,酸溶液中氢离子、碱溶液中的氢氧根离子浓度越大,水的电离程度越小;
B.稀释后醋酸的电离程度增大,则氢离子浓度大于1×10-5mol/L;
C.结合等体积混合时生成的醋酸钠溶液呈碱性分析;
D.醋酸为弱酸,pH相等时醋酸的浓度较大.
解答 解:A.0.1mol/LNaOH溶液中氢氧根离子浓度为0.1mol/L,pH=3CH3COOH溶液中氢离子浓度为0.1mol/L,溶液中氢离子、碱溶液中的氢氧根离子浓度越大,水的电离程度越小,则由水电离出H+的浓度c(H+):①<③,故A错误;
B.pH=3CH3COOH溶液加蒸馏水稀释至原来的100倍时,所得溶液中氢离子浓度大于1×10-5mol/L,则溶液的pH<5,故B错误;
C.①与③若等体积混合,二者恰好反应生成醋酸钠,醋酸根离子部分水解溶液呈碱性,若使反应后溶液呈中性,则加入醋酸的体积稍大,即:V(NaOH)<V(CH3COOH),故C错误;
D.等体积等pH的④溶液和盐酸,由于醋酸为弱酸,pH相等时醋酸的浓度较大,分别与足量的Zn反应时④溶液生成同条件下氢气体积多,故D正确;
故选D.
点评 本题考查酸碱混合的定性判断、弱电解质的电离平衡及其影响,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握弱电解质的电离特点,试题培养了学生的灵活应用能力.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
2.全氮类物质具有高密度、超高能量及爆轰产物无污染等优点.中国科学家成功合成全氮阴离子N5-,N5-是制备全氮类物质N5+N5-的重要中间体.下列说法中,不正确的是( )
| A. | 全氮类物质属于绿色能源 | B. | 每个N5+中含有35个质子 | ||
| C. | 每个N5-中含有35个电子 | D. | N5+N5-结构中含共价键 |
5.常温下,用浓度为0.1000mol/L的盐酸分别逐滴加入到20.00mL 0.1000mol/L的两种一元碱MOH、ROH溶液中,PH随盐酸溶液体积的变化如图所示.下列说法正确的是( )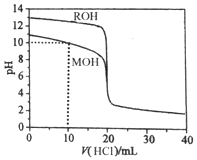

| A. | pH=10时,c(M+)>c(MOH)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时:c(R+)>c(M+)>c(H+)>c(OH-) | |
| C. | 10mL<V(HCl)<20mL时,c(M+)+c(MOH)<c(Cl-) | |
| D. | V(HCl)>20mL时,不可能存在:c(Cl-)>c(M+)=c(H+)>c(OH-) |
2.酚醛树脂材料具有绝缘、隔热、难燃等性能,合成酚醛树脂反应如图:
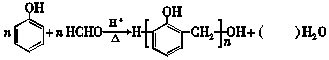
下列说法正确的是( )

下列说法正确的是( )
| A. | 方程式中水的化学计量数是 2n-1 | |
| B. | 常温下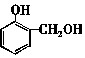 比 比 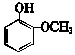 更难溶于水 更难溶于水 | |
| C. | 1 mol HCHO与银氨溶液反应最多可以生成2 mol Ag | |
| D. |  的单体是 的单体是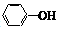 和HCHO 和HCHO |
3.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、A12O3、MnO等)制取CoCl2•6H2O的工艺流程如图1:
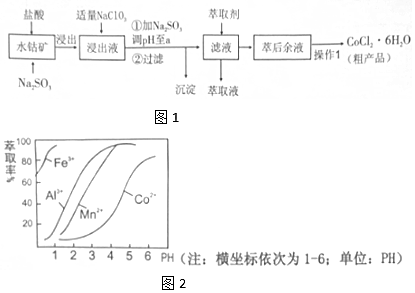
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L);
③CoCl2•6H2O熔点为86℃,加热至110〜120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)若不慎向“浸出液”中加过量NaClO2时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干需减压烘干的原因是降低烘干温度,防止产品分解.
(4)萃取剂对金属离子的萃取率与pH的关系如图2向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)为测定粗产品中CoCl2•6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L);
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)若不慎向“浸出液”中加过量NaClO2时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干需减压烘干的原因是降低烘干温度,防止产品分解.
(4)萃取剂对金属离子的萃取率与pH的关系如图2向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)为测定粗产品中CoCl2•6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答条即可)
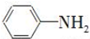 )有还原性,易被氧化;
)有还原性,易被氧化;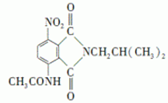 .
.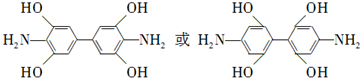 .
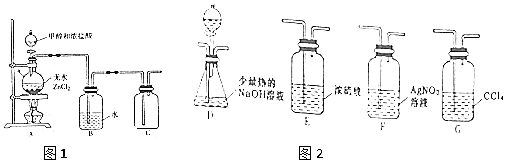
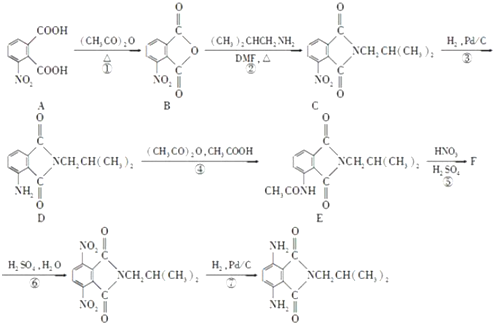
.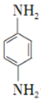 是一种重要的染料中间体.根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
是一种重要的染料中间体.根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用).合成路线流程图示例如下: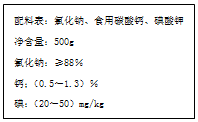 如图是某厂生产的某种加钙食盐包装标签上的部分文字,请阅读后回答以下问题:
如图是某厂生产的某种加钙食盐包装标签上的部分文字,请阅读后回答以下问题: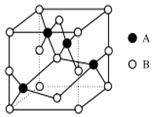 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物.回答下列问题: