题目内容
下列不是离子化合物的是( )
A、 |
B、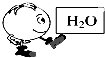 |
C、 |
D、 |
考点:离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,金属氧化物、大多数盐都是离子化合物,据此分析解答.
解答:
解:A.氯化钠是阴阳离子构成的,属于离子化合物,故A不选;
B.水分子是由氢原子和O原子构成的,属于共价化合物,故B选;
C.KOH是由钾离子和氢氧根离子构成的,氢氧根离子是由O原子和H原子构成的,所以KOH中存在离子键和共价键,属于离子化合物,故C不选;
D.硝酸钠是由钠离子和硝酸根离子构成的,硝酸根离子中存在共价键,所以硝酸钠属于离子化合物,故D不选;
故选B.
B.水分子是由氢原子和O原子构成的,属于共价化合物,故B选;
C.KOH是由钾离子和氢氧根离子构成的,氢氧根离子是由O原子和H原子构成的,所以KOH中存在离子键和共价键,属于离子化合物,故C不选;
D.硝酸钠是由钠离子和硝酸根离子构成的,硝酸根离子中存在共价键,所以硝酸钠属于离子化合物,故D不选;
故选B.
点评:本题考查化学键,明确离子键和共价键的区别是解本题关键,不能根据是否含有金属元素判断离子化合物,氯化铝中含有金属元素但为共价化合物,铵盐中只含非金属元素但为离子化合物,为易错点.

练习册系列答案
相关题目
下列有机物的系统命名正确的是( )
A、 异丁烷 |
B、 2-甲基-3-丁烯 |
C、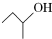 2-丁醇 |
D、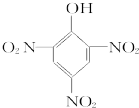 1,3,5-三硝基苯酚 |
F2、Cl2、Br2、I2的氧化性递变规律依次为( )
| A、逐渐减弱 | B、逐渐增强 |
| C、变化不大 | D、无法比较 |
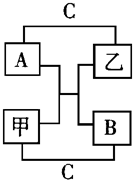 A、B、C是短周期里的3种元素的单质,甲、乙是常见的化合物,它们之间存在如图所示的转化关系:若A为有色气体,C 为无色气体,B为淡黄色固体,请回答:
A、B、C是短周期里的3种元素的单质,甲、乙是常见的化合物,它们之间存在如图所示的转化关系:若A为有色气体,C 为无色气体,B为淡黄色固体,请回答: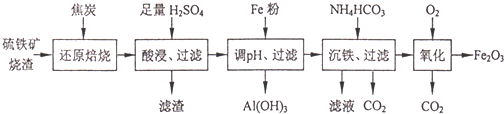

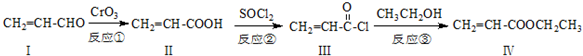
 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为