题目内容
在25℃下,取0.2mol?L-1 HX溶液与0.2mol?L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是( )
| A、混合溶液中由水电离出的c(OH-)小于0.2 mol?L-1 HX溶液中由水电离出的c(H+) |
| B、c(Na+)=c(X-)+c(HX)=0.2 mol?L-1 |
| C、c(Na+)-c(X-)=9.9×10-7 mol?L-1 |
| D、c(OH-)=c(HX)+c(H+)=1×10-8 mol?L-1 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:
分析:相同物质的量浓度和体积的一元酸和一元碱恰好反应生成盐和水,根据盐溶液的酸碱性判断酸的强弱;
A、含有弱根离子的盐能促进水的电离,酸或碱能抑制水的电离.
B、根据物料守恒确定离子之间的关系式.
C、根据电荷守恒计算钠离子和酸根离子的差.
D、根据物料守恒和电荷守恒判断氢氧根离子和酸、氢离子浓度的关系.
A、含有弱根离子的盐能促进水的电离,酸或碱能抑制水的电离.
B、根据物料守恒确定离子之间的关系式.
C、根据电荷守恒计算钠离子和酸根离子的差.
D、根据物料守恒和电荷守恒判断氢氧根离子和酸、氢离子浓度的关系.
解答:
解:取0.2mol?L-1 HX溶液与0.2mol?L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),一元酸和一元碱的物质的量相等,混合后测得混合溶液的pH=8,说明形成的盐是强碱弱酸盐水溶液呈碱性.
A、混合溶液是盐溶液,且该盐含有弱根离子所以能促进水的电离,酸或碱能抑制水的电离,所以混合溶液中由水电离出的c(OH-)大于0.2 mol?L-1 HX溶液中由水电离出的c(H+),故A错误.
B、溶液混合后,溶液的体积扩大1倍,离子的浓度缩小1倍,根据物料守恒知c(Na+)=c(X-)+c(HX)=0.1 mol?L-1,故B错误.
C、溶液呈电中性,所以C(H+)+C(Na+)=c(X-)+C(OH-),所以c(Na+)-c(X-)=C(OH-)-C(H+)=10-6 mol/L-10-8 mol/L=9.9×10-7 mol?L-1,故C正确.
D、根据物料守恒知c(Na+)=c(X-)+c(HX)=0.1 mol?L-1,根据电荷守恒得C(H+)+C(Na+)=c(X-)+C(OH-),所以c(OH-)=c(HX)+c(H+),溶液中氢离子浓度为10-8 mol/L,所以氢氧根离子浓度大于1×10-8 mol?L-1,故D错误.
故选C.
A、混合溶液是盐溶液,且该盐含有弱根离子所以能促进水的电离,酸或碱能抑制水的电离,所以混合溶液中由水电离出的c(OH-)大于0.2 mol?L-1 HX溶液中由水电离出的c(H+),故A错误.
B、溶液混合后,溶液的体积扩大1倍,离子的浓度缩小1倍,根据物料守恒知c(Na+)=c(X-)+c(HX)=0.1 mol?L-1,故B错误.
C、溶液呈电中性,所以C(H+)+C(Na+)=c(X-)+C(OH-),所以c(Na+)-c(X-)=C(OH-)-C(H+)=10-6 mol/L-10-8 mol/L=9.9×10-7 mol?L-1,故C正确.
D、根据物料守恒知c(Na+)=c(X-)+c(HX)=0.1 mol?L-1,根据电荷守恒得C(H+)+C(Na+)=c(X-)+C(OH-),所以c(OH-)=c(HX)+c(H+),溶液中氢离子浓度为10-8 mol/L,所以氢氧根离子浓度大于1×10-8 mol?L-1,故D错误.
故选C.
点评:本题考查了混合溶液中离子浓度大小的判断,难度较大,注意含有弱根离子的盐能促进水的电离,酸或碱能抑制水的电离.

练习册系列答案
相关题目
在元素周期表中,第一、二、三、四周期元素的种类分别是( )
| A、2、8、8、18 |
| B、2、8、18、18 |
| C、2、18、18、18 |
| D、2、8、18、32 |
2011年3月12日,日本福岛第一核电站由于地震原因而发生爆炸,造成放射性物质泄漏,核电站周围检测到铯137和碘131超标.核电站为阻止高辐射污水由碎石层流入竖井裂缝进入海中,向碎石层内注入“水玻璃”.几天后受“吃加碘盐能防止核辐射”等谣言的影响,我国部分地区出现抢购食盐现象.已知食盐中添加的碘盐为KIO3,下列说法正确的是( )
A、核素
| ||||
| B、“水玻璃”是硅酸钠的俗称,是一种黏合剂 | ||||
| C、KIO3中碘元素的化合价是+5,碘原子的最外层最多可排7个电子 | ||||
D、I和
|
根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价.
部分短周期元素的原子半径及主要化合价.
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、氢化物的沸点为HnT<HnQ |
| B、L、R的单质与稀盐酸反应的速率为R>L |
| C、M与T形成的化合物具有两性 |
| D、L、Q形成的简单离子的核外电子数相等 |

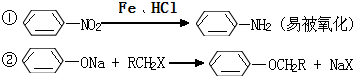
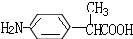 ).写出同时满足下列条件的F的两种同分异构体的结构简式:
).写出同时满足下列条件的F的两种同分异构体的结构简式: .写出以苯酚钠、CH3CH2OH和(CH3CO)2O为原料制备非那西汀的五步合成路线流程图(无机试剂任用).
.写出以苯酚钠、CH3CH2OH和(CH3CO)2O为原料制备非那西汀的五步合成路线流程图(无机试剂任用).
