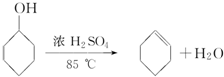
题目内容
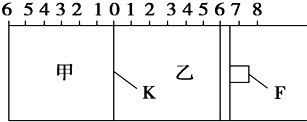
如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2mol SO2和1mol O2,乙中充入2mol SO3和1mol He,此时K停在0处.在一定条件下发生可逆反应:2SO2(g)+O2(g)?2SO3(g),反应达到平衡后,再恢复至原温度,回答下列问题:
(1)若固定隔板K,能表示甲容器中一定达到化学平衡的是
A.甲中气体的总压强不变 B.各气体的物质的量浓度不变
C.混合气体的平均摩尔质量不变 D.混合气体的密度不变
E.反应速率v(SO2)=v(SO3)
(2)达到平衡后隔板K是否可能处于0刻度 (填“可能”或“不可能”).若K最终停留在0刻度左侧a处,则a一定小于 .
(3)若平衡时,K最终停留在左侧刻度1处,则甲中SO3的物质的量为 mol,乙中SO3的转化率 50%(填“>”、“<”或“=”),活塞F最终停留在右侧刻度 处(填下列序号:①<6 ②>6 ③=6).
(4)若一开始就将K、F固定,其他条件均不变,甲平衡后压强变为开始压强的0.8倍,则甲、乙都达到平衡后,两容器的压强之比为P甲:P乙=
(1)若固定隔板K,能表示甲容器中一定达到化学平衡的是
A.甲中气体的总压强不变 B.各气体的物质的量浓度不变
C.混合气体的平均摩尔质量不变 D.混合气体的密度不变
E.反应速率v(SO2)=v(SO3)
(2)达到平衡后隔板K是否可能处于0刻度
(3)若平衡时,K最终停留在左侧刻度1处,则甲中SO3的物质的量为
(4)若一开始就将K、F固定,其他条件均不变,甲平衡后压强变为开始压强的0.8倍,则甲、乙都达到平衡后,两容器的压强之比为P甲:P乙=

考点:化学平衡状态的判断,化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:(1)根据平衡状态的特征,判断正逆反应速率是否相等;
(2)根据反应是气体体积减小的反应,可逆反应不能完全反应进行分析;
(3)“隔板K最终停留在左侧1处”说明反应后气体体积为5格,即物质的量为2.5mol,
设参加反应的二氧化硫的物质的量为2x,
故2-2x+1-x+2x=2.5,
则x=0.5mol,
则甲中二氧化硫的转化率为50%,生成三氧化硫物质的量为1mol;
但是对于乙来说,就不同了,如果无He,甲与乙是等效平衡,但乙的压强比甲小,则 2SO3(g)?2SO2(g)+O2(g)的平衡向右移动了;
(4)根据压强之比等于气体物质的量之比,依据极值分析判断;
(2)根据反应是气体体积减小的反应,可逆反应不能完全反应进行分析;
(3)“隔板K最终停留在左侧1处”说明反应后气体体积为5格,即物质的量为2.5mol,
设参加反应的二氧化硫的物质的量为2x,
故2-2x+1-x+2x=2.5,
则x=0.5mol,
则甲中二氧化硫的转化率为50%,生成三氧化硫物质的量为1mol;
但是对于乙来说,就不同了,如果无He,甲与乙是等效平衡,但乙的压强比甲小,则 2SO3(g)?2SO2(g)+O2(g)的平衡向右移动了;
(4)根据压强之比等于气体物质的量之比,依据极值分析判断;
解答:
解:(1)A.甲中气体的总压强不变,说明正逆反应速率相等,达平衡状态,故正确;
B.各气体的物质的量浓度不变,说明正逆反应速率相等,达平衡状态,故正确;
C.混合气体的平均摩尔质量不变,说明正逆反应速率相等,达平衡状态,故正确;
D.混合气体的密度不变,始终不变,故错误;
E.反应速率v(SO2)=v(SO3),未体现正逆的关系,故错误;
故选:ABC;
(2)2SO2(g)+O2(g)?2SO3(g),反应是气体体积减小的反应,隔板一定发生滑动,达到平衡后隔板K不可能处于0刻度;由于甲中充入2molSO2和1mol O2,反应向正反应方向移动,A中压强降低,最多能转化为2mol SO3,但是由于反应是可逆反应,所以2SO3的物质的量在0-2 mol之间,所以达到平衡后,隔板K不再滑动,最终停留在左侧刻度0-2之间,故a小于2,故答案为:不可能,2;
(3)由于左右两边不考虑加入的氦气,达到的平衡是相同平衡,三氧化硫体积分数相同,“隔板K最终停留在左侧1处”说明反应后气体体积为5格,左边气体减少了0.5mol,即平衡后物质的量为2.5mol,
设参加反应的二氧化硫的物质的量为2x,
故2-2x+1-x+2x=2.5,
则x=0.5mol,
则甲中二氧化硫的转化率为50%.生成三氧化硫物质的量为1mol;
但是对于乙来说,就不同了,如果无He,甲与乙是等效平衡,但乙的压强比甲小,则2SO3(g)?2SO2(g)+O2(g)的平衡向右移动了,故其转化率比大于50%;左边气体减少了0.5mol,右边增加物质的量大于0.5mol,F活塞右移,活塞F最终停留在右侧刻度大于6处;
故答案为:1,>,②;
(4)两个容器达平衡时是等效平衡,甲平衡后压强变为开始压强的0.8倍,平衡时物质的量为3×0.8=2.4mol,则乙都达到平衡时物质的量为2.4mol+1mol=3.4mol,所以两容器的压强之比为P甲:P乙=2.4:3.4=12:17,故答案为:12:17.
B.各气体的物质的量浓度不变,说明正逆反应速率相等,达平衡状态,故正确;
C.混合气体的平均摩尔质量不变,说明正逆反应速率相等,达平衡状态,故正确;
D.混合气体的密度不变,始终不变,故错误;
E.反应速率v(SO2)=v(SO3),未体现正逆的关系,故错误;
故选:ABC;
(2)2SO2(g)+O2(g)?2SO3(g),反应是气体体积减小的反应,隔板一定发生滑动,达到平衡后隔板K不可能处于0刻度;由于甲中充入2molSO2和1mol O2,反应向正反应方向移动,A中压强降低,最多能转化为2mol SO3,但是由于反应是可逆反应,所以2SO3的物质的量在0-2 mol之间,所以达到平衡后,隔板K不再滑动,最终停留在左侧刻度0-2之间,故a小于2,故答案为:不可能,2;
(3)由于左右两边不考虑加入的氦气,达到的平衡是相同平衡,三氧化硫体积分数相同,“隔板K最终停留在左侧1处”说明反应后气体体积为5格,左边气体减少了0.5mol,即平衡后物质的量为2.5mol,
设参加反应的二氧化硫的物质的量为2x,
故2-2x+1-x+2x=2.5,
则x=0.5mol,
则甲中二氧化硫的转化率为50%.生成三氧化硫物质的量为1mol;
但是对于乙来说,就不同了,如果无He,甲与乙是等效平衡,但乙的压强比甲小,则2SO3(g)?2SO2(g)+O2(g)的平衡向右移动了,故其转化率比大于50%;左边气体减少了0.5mol,右边增加物质的量大于0.5mol,F活塞右移,活塞F最终停留在右侧刻度大于6处;
故答案为:1,>,②;
(4)两个容器达平衡时是等效平衡,甲平衡后压强变为开始压强的0.8倍,平衡时物质的量为3×0.8=2.4mol,则乙都达到平衡时物质的量为2.4mol+1mol=3.4mol,所以两容器的压强之比为P甲:P乙=2.4:3.4=12:17,故答案为:12:17.
点评:本题考查了化学平衡的建立过程分析判断,注意恒温容器和恒压容器中的平衡特征分析,掌握反应过程中的气体变化和平衡建立是解题关键,题目难度较大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
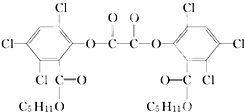 夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )
夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )| A、草酸二酯的分子式为C26H24Cl6O8 |
| B、1 mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4 mol NaOH |
| C、该有机物能发生加成反应、取代反应、氧化反应 |
| D、1 mol草酸二酯与氢气完全反应,需要氢气6 mol |
已知某温度下,Ka(HCN)=6.2×10-10mol/L、Ka(HF)=6.8×10-4 mol/L、Ka(CH3COOH)=1.8×10-5 mol/L、Ka(HNO2)=6.4×10-6 mol/L.物质的量浓度都为0.1mol/L的下列溶液中,酸性最强的是( )
| A、HCN溶液 |
| B、HF溶液 |
| C、CH3COOH溶液 |
| D、HNO2溶液 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2O4+8H2O
3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是( )
| 放电 |
| 充电 |
| A、放电时负极反应为:3Zn-6e-+6OH-═3Zn(OH)2 |
| B、放电时正极反应为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH- |
| C、放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D、放电时正极附近溶液的碱性增强 |
将淀粉氯化钾混合溶液装在羊皮纸制成的半透膜袋中,将此袋下半部浸泡在盛有蒸馏水的烧杯里,过一段时间后进行实验.下列现象能证明羊皮纸袋一定有破损的是( )
| A、取羊皮纸袋内液体加入碘水变蓝色 |
| B、取烧杯中液体加入KI溶液不变蓝色 |
| C、取烧杯中液体加入AgNO3溶液产生黄色沉淀 |
| D、取烧杯中液体加入碘水变蓝色 |
下列各组离子在相应的条件下可能大量共存的是( )
| A、能使pH试纸变红的溶液中:CO32-、Ba2+、Cl-、Na+ | ||
| B、由水电离产生的c(OH-)=1×10-10 mol/L的溶液中:NO3-、Mg2+、SO42-、Fe2+ | ||
C、在
| ||
| D、无色透明溶液中:Al3+、HCO3-、Cl-、K+ |
下列各物质的溶液物质的量浓度均为0.1mol/L:①HCl;②NaOH;③Na2CO3;④NH4Cl;⑤CH3COONa;⑥Ba(OH)2;⑦KCl.它们pH按由小到大的排列顺序为( )
| A、⑥②③⑤⑦④① |
| B、①④⑦③⑤②⑥ |
| C、①④⑤③⑦②⑥ |
| D、①④⑦⑤③②⑥ |