题目内容
取一定量可能含有Cu(NO3)2、AgNO3、KNO3三种物质中的一种或多种成分的粉末,加热后得到A气体aL,将气体用足量的水吸收,剩余气体B的体积为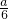 L.下列相关推测正确的是
L.下列相关推测正确的是
- A.NO2与O2的体积比为5:1
- B.气体B可能是NO2
- C.NO2与O2的体积比为2:1
- D.固体粉末的组成为n[Cu(NO3)2]:n(AgNO3):n(KNO3)=1:3:1
CD
分析:KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解化学方程式如下:①2KNO3 2KNO2+O2↑;
2KNO2+O2↑;
②2Cu(NO3)2 2CuO+4NO2↑+O2↑;
2CuO+4NO2↑+O2↑;
③2AgNO3 2Ag+2NO2↑+O2↑;
2Ag+2NO2↑+O2↑;
NO2与O2在水中反应的化学方程式如下:④4NO2+O2+2H2O═4HNO3,剩余气体可能为NO或O2,根据方程式讨论计算.
解答:KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解化学方程式如下:①2KNO3 2KNO2+O2↑;
2KNO2+O2↑;
②2Cu(NO3)2 2CuO+4NO2↑+O2↑;
2CuO+4NO2↑+O2↑;
③2AgNO3 2Ag+2NO2↑+O2↑;
2Ag+2NO2↑+O2↑;
NO2与O2在水中反应的化学方程式如下:④4NO2+O2+2H2O═4HNO3,剩余气体可能为NO或O2,
如剩余气体为O2,设反应的O2为xL,
4NO2+O2+2H2O═4HNO3
4 1
4x x
则4x+x=a-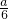 =
= ,
,
x=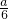 ,
,
NO2与O2的体积比为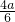 :
: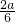 =2:1,
=2:1,
由反应的方程式可知,应满足:n[Cu(NO3)2]:n(KNO3)=1:1,n(AgNO3)可任意组成;
如剩余气体为NO,设反应的O2为yL,
3NO2+H2O═2HNO3+NO
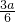 L
L 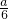 L
L
4NO2+O2+2H2O═4HNO3
4 1
4y y
5y=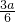
y=0.1a,
则NO2与O2的体积比为(0.4a+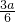 ):0.1a=9:1,
):0.1a=9:1,
但是根据这些固体加热产生的NO2和O2的比例来看,生成的NO2与O2物质的量之比为9:1是不可能的,
因此:剩余气体只能为O2,且NO2与O2的体积比为2:1,混合物应应满足:n[Cu(NO3)2]:n(KNO3)=1:1,n(AgNO3)可任意组成,
故选CD.
点评:本题考查混合物的计算,题目难度较大,解答时注意反应的化学方程式,判断分解产物的气体之间的体积关系,为解答该题的关键点,也是易错点.
分析:KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解化学方程式如下:①2KNO3
 2KNO2+O2↑;
2KNO2+O2↑;②2Cu(NO3)2
 2CuO+4NO2↑+O2↑;
2CuO+4NO2↑+O2↑;③2AgNO3
 2Ag+2NO2↑+O2↑;
2Ag+2NO2↑+O2↑;NO2与O2在水中反应的化学方程式如下:④4NO2+O2+2H2O═4HNO3,剩余气体可能为NO或O2,根据方程式讨论计算.
解答:KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解化学方程式如下:①2KNO3
 2KNO2+O2↑;
2KNO2+O2↑;②2Cu(NO3)2
 2CuO+4NO2↑+O2↑;
2CuO+4NO2↑+O2↑;③2AgNO3
 2Ag+2NO2↑+O2↑;
2Ag+2NO2↑+O2↑;NO2与O2在水中反应的化学方程式如下:④4NO2+O2+2H2O═4HNO3,剩余气体可能为NO或O2,
如剩余气体为O2,设反应的O2为xL,
4NO2+O2+2H2O═4HNO3
4 1
4x x
则4x+x=a-
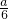 =
= ,
,x=
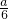 ,
,NO2与O2的体积比为
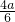 :
: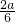 =2:1,
=2:1,由反应的方程式可知,应满足:n[Cu(NO3)2]:n(KNO3)=1:1,n(AgNO3)可任意组成;
如剩余气体为NO,设反应的O2为yL,
3NO2+H2O═2HNO3+NO
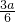 L
L 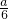 L
L4NO2+O2+2H2O═4HNO3
4 1
4y y
5y=
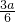
y=0.1a,
则NO2与O2的体积比为(0.4a+
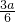 ):0.1a=9:1,
):0.1a=9:1,但是根据这些固体加热产生的NO2和O2的比例来看,生成的NO2与O2物质的量之比为9:1是不可能的,
因此:剩余气体只能为O2,且NO2与O2的体积比为2:1,混合物应应满足:n[Cu(NO3)2]:n(KNO3)=1:1,n(AgNO3)可任意组成,
故选CD.
点评:本题考查混合物的计算,题目难度较大,解答时注意反应的化学方程式,判断分解产物的气体之间的体积关系,为解答该题的关键点,也是易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
取一定量可能含有Cu(NO3)2、AgNO3、KNO3三种物质中的一种或多种成分的粉末,加热后得到A气体a L,将气体用足量的水吸收,剩余气体B的体积为a/6 L。下列相关推测正确的是
| A.NO2与O2的体积比为5:1 |
| B.气体B可能是NO2 |
| C.NO2与O2的体积比为2:1 |
| D.固体粉末的组成为n[Cu(NO3)2]:n(AgNO3):n(KNO3)=1:3:1 |
 L.下列相关推测正确的是( )
L.下列相关推测正确的是( )