题目内容
18g某混合气体通过足量的Na2O2固体充分反应后固体增重2g,则该混合气体不可能是( )
| A、H2O、O2 |
| B、CO2、H2 |
| C、CO2、H2O、O2 |
| D、CO2、CO |
考点:有关混合物反应的计算
专题:
分析:根据2Na2O2+2CO2=2Na2CO3+O2知,反应前后固体质量增加量相当于CO,假设气体完全是二氧化碳,固体质量增加2g时,m(CO2)=
×1×44g/mol=3.14g;
根据2Na2O2+2H2O=4NaOH+O2↑知,反应前后固体质量增加量相当于氢气,假设气体完全是水蒸气,固体质量增加2g时,m(H2O)=
×1×18g/mol=18g,
如果气体和过氧化钠不反应,则过氧化钠固体质量不增加,相当于需要气体质量无穷大,
根据气体质量和固体增加质量进行计算.
| ||
| 1 |
根据2Na2O2+2H2O=4NaOH+O2↑知,反应前后固体质量增加量相当于氢气,假设气体完全是水蒸气,固体质量增加2g时,m(H2O)=
| ||
| 1 |
如果气体和过氧化钠不反应,则过氧化钠固体质量不增加,相当于需要气体质量无穷大,
根据气体质量和固体增加质量进行计算.
解答:
解:根据2Na2O2+2CO2=2Na2CO3+O2知,反应前后固体质量增加量相当于CO,假设气体完全是二氧化碳,固体质量增加2g时,m(CO2)=
×1×44g/mol=3.14g;
根据2Na2O2+2H2O=4NaOH+O2↑知,反应前后固体质量增加量相当于氢气,假设气体完全是水蒸气,固体质量增加2g时,m(H2O)=
×1×18g/mol=18g,
如果气体和过氧化钠不反应,则过氧化钠固体质量不增加,
A.根据以上知,如果混合气体是水蒸气和氧气,氧气和过氧化钠不反应,水蒸气和过氧化钠反应,当固体质量增加2g时,水蒸气的质量是18g,所以氧气的量为0,不符合条件,故A选;
B.如果是氢气和二氧化碳,氢气和过氧化钠不反应,固体质量增加2g时需要气体质量无穷大,需要二氧化碳3.14g,18g介于二者之间,所以能实现18g该混合气体通过足量的Na2O2固体充分反应后固体增重2g,故B不选;
C.当混合气体是CO2、H2O、O2,氧气和过氧化钠不反应,相当于需要氧气的质量无穷大,过氧化钠增加2g时需要水蒸气18g,需要二氧化碳质量为3.14g,则混合气体质量18g介于氧气质量和二氧化碳质量之间,所以能实现该目的,故C不选;
D.固体质量增加2g时,CO和过氧化钠不反应,相当于需要CO质量无穷大,需要二氧化碳质量3.14g,18g介于无穷大和3.14g之间,所以该混合气体能实现该目的,故D不选;
故选A.
| ||
| 1 |
根据2Na2O2+2H2O=4NaOH+O2↑知,反应前后固体质量增加量相当于氢气,假设气体完全是水蒸气,固体质量增加2g时,m(H2O)=
| ||
| 1 |
如果气体和过氧化钠不反应,则过氧化钠固体质量不增加,
A.根据以上知,如果混合气体是水蒸气和氧气,氧气和过氧化钠不反应,水蒸气和过氧化钠反应,当固体质量增加2g时,水蒸气的质量是18g,所以氧气的量为0,不符合条件,故A选;
B.如果是氢气和二氧化碳,氢气和过氧化钠不反应,固体质量增加2g时需要气体质量无穷大,需要二氧化碳3.14g,18g介于二者之间,所以能实现18g该混合气体通过足量的Na2O2固体充分反应后固体增重2g,故B不选;
C.当混合气体是CO2、H2O、O2,氧气和过氧化钠不反应,相当于需要氧气的质量无穷大,过氧化钠增加2g时需要水蒸气18g,需要二氧化碳质量为3.14g,则混合气体质量18g介于氧气质量和二氧化碳质量之间,所以能实现该目的,故C不选;
D.固体质量增加2g时,CO和过氧化钠不反应,相当于需要CO质量无穷大,需要二氧化碳质量3.14g,18g介于无穷大和3.14g之间,所以该混合气体能实现该目的,故D不选;
故选A.
点评:本题考查混合物的计算,明确物质之间不反应时相当于需要该气体质量无穷大是解本题关键,混合气体质量介于二者之间的就符合条件,侧重考查分析、计算能力,题目难度中等.

练习册系列答案
相关题目
一定温度下,在一个容积可变的密闭容器中,发生C(s)+H2O(g)?CO(g)+H2(g)反应,下列能判断该反应达到化学平衡状态的是( )
| A、容器中的压强不变 |
| B、2 mol H-O键断裂的同时1 mol H-H键形成 |
| C、c(CO)=c(H2) |
| D、密闭容器的容积不再改变 |
25℃时,往浓度都为0.1mol?L-1的氨水和氢氧化钠混合溶液中滴加0.1mol?L-1的某一元酸HA,下列说法正确的是( )
| A、当加入HA至溶液pH=7时,溶液中的碱还未反应完 |
| B、在滴加HA的过程中,水的电离程度先减小后增加 |
| C、在滴加HA的过程中,溶液中可能存在如下浓度关系:c(A-)>c(Na+)>c(NH4+)>c(H+)>c(OH-) |
| D、反应到达终点时:c(NH4+)+c(NH3?H2O)=0.1mol?L-1 |
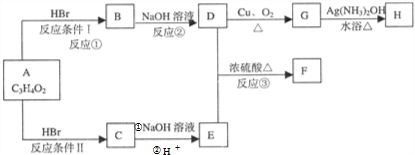
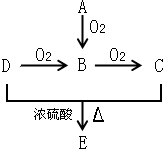 已知A、B、C、D和E五种有机物存在如图所示的转化关系.A是一种标准状况下密度为1.25g.L-1的烃,E是一种有水果香味的有机物.
已知A、B、C、D和E五种有机物存在如图所示的转化关系.A是一种标准状况下密度为1.25g.L-1的烃,E是一种有水果香味的有机物.