题目内容
6.若20g密度为ρg•cm-3的硝酸钙溶液里含1gCa2+,则NO3-的物质的量浓度是( )| A. | 400ρmol•L-1 | B. | 20ρmol•L-1 | C. | 2.5ρmol•L-1 | D. | 1.25ρmol•L-1 |
分析 先根据V=$\frac{m}{ρ}$计算出该硝酸钙溶液的体积,再根据c=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$计算出该溶液中钙离子的浓度,最后根据硝酸钙的化学式组成计算出溶液中NO3-的物质的量浓度.
解答 解:20g密度为ρg•cm-3的硝酸钙溶液的体积为:$\frac{20g}{ρg•c{m}^{-3}}$=$\frac{20}{ρ}$mL=$\frac{20}{ρ}$×10-3L,
1gCa2+的物质的量为:n(Ca2+)=$\frac{1g}{40g/mol}$=0.025mol,
该溶液中钙离子的物质的量浓度为:c(Ca2+)=$\frac{0.025mol}{\frac{20}{ρ}×1{0}^{-3}L}$=1.25ρmol/L,
该溶液中NO3-的物质的量浓度为:c(NO3-)=2c(Ca2+)=1.25ρmol/L×2=2.5ρmol/L,
故选C.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及化学计算能力.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
16.下列叙述正确的是( )
| A. | 标准状况下,22.4LSO3中含有氧原子的数目为3NA | |
| B. | 18gH218O 中含有的电子数为10NA | |
| C. | 常温下,4g甲烷中含有C-H键的数目为NA | |
| D. | 24g镁原子最外层电子数为NA |
17.下列关于化学用语的表述正确的是( )
| A. | 丙烷分子的球棍模型: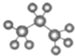 | B. | S的结构示意图为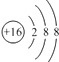 | ||
| C. | HClO的结构式为H-Cl-O | D. | 碳-14核素:814C |
14.下列说法正确的是( )
| A. | 不能发生丁达尔效应的分散系有氯化钠溶液、水等 | |
| B. | 将1L 2mol•L-1的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA | |
| C. | 黄河入海口处三角洲的形成与胶体性质有关 | |
| D. | 将饱和FeCl3溶液加热至沸腾,制得Fe(OH)3胶体 |
1.当压力达到220个大气压、温度达到374℃时,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源.下列说法不正确的是( )
| A. | 二氧化碳与超临界水作用生成汽油的反应,属于放热反应 | |
| B. | “水热反应”是一种复杂的物理化学变化 | |
| C. | 火力发电厂可以利用废热,将二氧化碳转变为能源物质 | |
| D. | 随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环 |
11.我市中考实行网上阅卷.答题时必须用2B铅笔填涂答题卡,2B铅笔芯的主要成分是( )
| A. | 石墨 | B. | 金刚石 | C. | 木炭 | D. | C60 |
18.下列说法正确的是( )
| A. | 石油、煤、天然气都属于化石燃料 | |
| B. | 自发反应一定是熵增大,非自发反应一定是熵减小 | |
| C. | “冰,水为之,而寒于水”说明相同质量的水和冰,冰的能量高 | |
| D. | SiO2既能溶于NaOH溶液又能溶于HF溶液,说明SiO2是两性氧化物 |
15.已知X、Y、Z、R、W均为元素周期表中短周期主族元素.它们在周期表中的相对位置如图所示.下列说法正确的是( )
| X | |||
| Y | Z | R | W |
| A. | 该五种元素一定为非金属元素 | |
| B. | 元素Y、Z、R的氧化物一定属于三种不同类型的晶体 | |
| C. | Z的原子序数可能是X的两倍 | |
| D. | W的最高价氧化物对应的水化物可能是最强的无机含氧酸 |
12.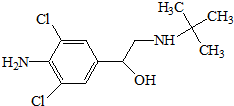 瘦肉精,学名盐酸克伦特罗,该药物既不是兽药,也不是饲料添加剂,而是肾上腺类神经兴奋剂,可以增加动物的瘦肉量.减少饲料使用.使肉品提早上市,降低成本,但对人体会产生副作用,盐酸克伦特罗分子结构简式如图.下列说法不正确的是( )
瘦肉精,学名盐酸克伦特罗,该药物既不是兽药,也不是饲料添加剂,而是肾上腺类神经兴奋剂,可以增加动物的瘦肉量.减少饲料使用.使肉品提早上市,降低成本,但对人体会产生副作用,盐酸克伦特罗分子结构简式如图.下列说法不正确的是( )
 瘦肉精,学名盐酸克伦特罗,该药物既不是兽药,也不是饲料添加剂,而是肾上腺类神经兴奋剂,可以增加动物的瘦肉量.减少饲料使用.使肉品提早上市,降低成本,但对人体会产生副作用,盐酸克伦特罗分子结构简式如图.下列说法不正确的是( )
瘦肉精,学名盐酸克伦特罗,该药物既不是兽药,也不是饲料添加剂,而是肾上腺类神经兴奋剂,可以增加动物的瘦肉量.减少饲料使用.使肉品提早上市,降低成本,但对人体会产生副作用,盐酸克伦特罗分子结构简式如图.下列说法不正确的是( )| A. | 瘦肉精的分子式是C11H18ON2Cl2 | |
| B. | 物质能发生取代反应、氧化反应、加成反应和水解反应 | |
| C. | 1mol盐酸克伦特罗最多能与4molNaOH反应 | |
| D. | 盐酸克伦特罗分子中至少有7个碳原子共面 |