题目内容
6.在原子序数1-18号元素中:(1)与水反应最剧烈的金属是Na(填化学式).
(2)与水反应最剧烈的非金属单质是F2(填化学式).
(3)气态氢化物最稳定的是HF(填化学式).
(4)最高价氧化物对应水化物的酸性最强的元素是HClO4(填元素符号).
分析 元素周期表中的递变规律:同周期元素的原子,从左到右,元素的金属性减弱,非金属性增强;氢化物稳定性增强;原子半径逐渐减小;最高价氧化物对应水化物的酸性逐渐增强;从下到上,元素的金属性减弱,非金属性增强;氢化物稳定性增强;原子半径逐渐减小;最高价氧化物对应水化物的酸性逐渐增强,以此解答该题.
解答 解:(1)与水反应最剧烈的金属是位于左下角的金属,在原子序数1-18号元素中应该是Na,故答案为:Na;
(2)与水反应最剧烈的非金属单质是位于最右上角的非金属单质,在原子序数1-18号元素中为F2,故答案为:F2;
(3)气态氢化物最稳定的物质位于周期表的最右上方,化学式是HF,故答案为:HF;
(4)周期表中,从下到上,最高价氧化物对应水化物的酸性逐渐增强,同周期元素的原子,从左到右,最高价氧化物对应水化物的酸性增强,所以最高价氧化物对应水化物的酸性最强的酸是高氯酸,故答案为:HClO4.
点评 本题考查学生元素周期表中的递变规律,为高频考点,侧重考查学生的分析能力,注意知识的归纳和整理是解题的关键,难度不大.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
16.下列说法正确的是( )
| A. | 1mol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| B. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| C. | 欲检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2并加热 | |
| D. | 油脂不是高分子化合物,1mol油脂完全水解生成1mol甘油和3mol高级脂肪酸 |
17.已知反应物的总能量低于产物的总能量,则反应是( )
| A. | 放热反应 | B. | 吸热反应 | C. | 有催化剂作用 | D. | 无法判断 |
14.如图是滴定管和量筒的两个液面.下列有关读数中正确的是( )
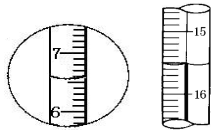

| A. | 左边是量筒读数6.5mL,右边是滴定管读数16.50mL | |
| B. | 左边是量筒读数7.5mL,右边是滴定管读数16.50mL | |
| C. | 左边是量筒读数6.5mL,右边是滴定管读数15.50mL | |
| D. | 左边是量简读数6.5mL,右边是滴定管读数16.50mL |
1. 一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?2C(g)△H<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2,下列有关说法正确的是( )
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?2C(g)△H<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2,下列有关说法正确的是( )
 一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?2C(g)△H<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2,下列有关说法正确的是( )
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?2C(g)△H<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2,下列有关说法正确的是( )| A. | 反应开始2min内,v(A)=0.025mol/(L•mol) | |
| B. | t1时改变的条件可能是升高温度 | |
| C. | t3时改变的条件可能是加压,此时c(B)不变 | |
| D. | t4时可能是使用了催化剂,此时c(B)不变 |
4.下列实验操作能达到实验目的是( )
| A. | 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 | |
| B. | 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO | |
| C. | SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物 | |
| D. | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性 |
8.金属钒主要用于冶炼特种钢和在化学工业、炼油工业中作催化剂,被誉为“合金的维生素”.回收利用废钒催化剂(主要成分为V2O5、VOSO4和二氧化硅)的工艺流程如图所示.

(1)粉碎的作用是提高VOSO4(可溶性钒化合物)的浸出率,滤渣可用于制作光导纤维、建筑材料等(填用途).
(2)25时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如表所示:
根据表数据判断,加入氨水调节溶液pH的最佳选择为1.7-1.8;上述过滤操作过程中所需用到的玻璃仪器有漏斗、烧杯、玻璃棒.
(3)为了提高钒的浸出率,用酸浸使废钒催化剂中的V2O5转变成可溶于水的VOSO4,酸浸过程中还原产物和氧化产物的物质的量之比为2:1.
(4)完成并配平氧化过程中的离子方程式:
1ClO3-+6VO2++6H+=6VO3++1Cl-+3H2O.
(5)废钒催化剂中V2O5的质量分数为6%(原料中的所有钒已换算成V2O5).取100g此废钒催化剂按上述流程进行实验,当加入105mL 0.1mol•L-1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该工业生产中钒的回收率是95.55%.

(1)粉碎的作用是提高VOSO4(可溶性钒化合物)的浸出率,滤渣可用于制作光导纤维、建筑材料等(填用途).
(2)25时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如表所示:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 9.8 | 96.4 | 93.0 | 89.3 |
(3)为了提高钒的浸出率,用酸浸使废钒催化剂中的V2O5转变成可溶于水的VOSO4,酸浸过程中还原产物和氧化产物的物质的量之比为2:1.
(4)完成并配平氧化过程中的离子方程式:
1ClO3-+6VO2++6H+=6VO3++1Cl-+3H2O.
(5)废钒催化剂中V2O5的质量分数为6%(原料中的所有钒已换算成V2O5).取100g此废钒催化剂按上述流程进行实验,当加入105mL 0.1mol•L-1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该工业生产中钒的回收率是95.55%.
9.A元素原子的核电荷数为11,B元素的质子数为8,A和B化合形成化合物Z,下列说法中错误的是( )
| A. | A可以形成+1价阳离子 | B. | B的最高价为+6价 | ||
| C. | Z一定可以与水反应 | D. | Z中不可能含有共价键 |
