题目内容
5.运用元素周期律分析下面的推断,其中错误的是( )| A. | 铍的氧化物的水化物可能具有两性 | |
| B. | 砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸 | |
| C. | 氢氧化铷[RbOH]易溶于水 | |
| D. | 硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
分析 A.Be与Al位于对角线位置;
B.同主族元素的单质及化合物性质相似;
C.碱金属从上到下对应碱的碱性增强,易溶于水;
D.同主族从上到下非金属性减弱.
解答 解:A.铍和Al位于对角线位置,氢氧化铝具有两性,则铍的氧化物的水化物可能具有两性,故A正确;
B.由同主族化合物性质相似可知,HAt不稳定,AgAt感光性强,但不溶于水也不溶于稀酸,但At为第六周期ⅦA族元素,卤族元素随电子层数的增多,单质的颜色不断加深,所以砹为有色固体,故B正确;
C.碱金属从上到下对应碱的碱性增强,易溶于水,则氢氧化铷[RbOH]易溶于水,故C正确;
D.硒是第四周期第VI A族元素,硒化氢的性质与H2S相似,但非金属性S强,没有H2S稳定,故D错误.
故选D.
点评 本题考查元素周期律和元素周期表,为高频考点,把握元素在元素周期表中的位置和元素周期律性质的递变规律为解答的关键,注意将不熟悉的元素和熟悉的元素相比较,从而得出结论,题目难度不大.

练习册系列答案
相关题目
16.下列关于常见有机物的说法正确的是( )
| A. | 甲烷、乙烯和苯都可以从化石燃料中获得,都能使溴水褪色 | |
| B. | 乙烯和苯分子都存在碳碳双键,因而都能发生加成反应和氧化反应 | |
| C. | 酸性高锰酸钾溶液既能鉴别乙烷和乙烯,也能除去乙烷中的乙烯,得到纯净的乙烷 | |
| D. | 乙醇、乙酸和乙酸乙酯能用饱和碳酸钠溶液鉴别 |
16.有甲、乙两个装置,下列说法错误的是( )


| A. | 甲、乙装置中,Zn的质量均减小 | B. | 甲、乙装置中,Cu上均有气泡产生 | ||
| C. | 化学反应速率 乙>甲 | D. | 甲中H+移向Zn,乙中SO42-移向Zn |
13.对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 达到化学平衡时:5v正(O2)=4v正(NO) | |
| B. | 达到化学平衡时:4v正(O2)=5 v逆(NO) | |
| C. | 任何时候化学反应速率关系:2v逆(NH3)=3v正(H2O) | |
| D. | 任何时候化学反应速率关系:2v逆(NH3)=3v逆(H2O) |
20.下列元素中,属于第三周期的是( )
| A. | 硅 | B. | 碳 | C. | 氮 | D. | 氢 |
17.分类是化学研究中常用的方法.下列分类方法中,不正确的是( )
| A. | 依据分散质微粒的大小,可将化合物分为酸、碱、盐等 | |
| B. | 依据电子转移与否,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 依据化合物本身在熔融状态或化合物的水溶液是否导电,可将其分为电解质和非电解质 | |
| D. | 依据组成元素的种类,将纯净物分为单质和化合物 |
14.除去氯化铁中混有的氯化铝,最适宜的试剂组是( )
| A. | NaOH溶液、盐酸 | B. | NaOH溶液、硫酸 | C. | 氨水、NaOH溶液 | D. | 氨水、盐酸 |
15.锌-碳硫酸原电池(如图)工作时,下列叙述正确的是( )
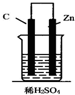

| A. | 正极反应为:Zn-2e-═Zn2+ | |
| B. | 电池反应式为:Zn+2H+═Zn2++H2↑ | |
| C. | 在闭合电路中,电子从碳极流向锌极 | |
| D. | 溶液中的H+移向锌极 |