题目内容
下列离子方程式书写正确的是( )
| A、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| B、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| C、三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| D、氯化铁溶液与氢氧化钠溶液:Fe3++3OH-═Fe(OH)3↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.转移电子不守恒、原子不守恒;
B.一水合氨是弱电解质;
C.电荷不守恒;
D.氯化铁和氢氧化钠溶液反应生成红褐色氢氧化铁沉淀.
B.一水合氨是弱电解质;
C.电荷不守恒;
D.氯化铁和氢氧化钠溶液反应生成红褐色氢氧化铁沉淀.
解答:
解:A.转移电子不守恒、原子不守恒,离子方程式为2H2O+2Al+2OH-═2AlO2-+3H2↑,故A错误;
B.一水合氨是弱电解质,离子方程式为:Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故B错误;
C.电荷不守恒,离子方程式为2Fe3++Fe=3Fe2+,故C错误;
D.氯化铁和氢氧化钠溶液反应生成红褐色氢氧化铁沉淀,离子方程式为Fe3++3OH-═Fe(OH)3↓,故D正确;
故选D.
B.一水合氨是弱电解质,离子方程式为:Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故B错误;
C.电荷不守恒,离子方程式为2Fe3++Fe=3Fe2+,故C错误;
D.氯化铁和氢氧化钠溶液反应生成红褐色氢氧化铁沉淀,离子方程式为Fe3++3OH-═Fe(OH)3↓,故D正确;
故选D.
点评:本题考查了离子方程式的书写,气体、沉淀、弱电解质、氧化物等物质要写化学式,有的反应与反应物的量有关,反应物的量不同,其离子方程式不同,还要遵循客观事实、原子守恒、电荷守恒、转移电子守恒,题目难度中等.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
查阅资料可知,苯可被臭氧氧化,发生如下化学反应: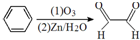 则二甲苯通过上述反应得到的产物有( )种.
则二甲苯通过上述反应得到的产物有( )种.
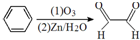 则二甲苯通过上述反应得到的产物有( )种.
则二甲苯通过上述反应得到的产物有( )种.| A、1 | B、2 | C、3 | D、4 |
下列应用涉及氧化还原反应的是( )
| A、粗盐提纯 | B、人工固氮 |
| C、工业制氧 | D、玻璃刻字 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水和海水之间含盐量的差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是( )
| A、Ag发生还原反应 |
| B、正极反应式:5MnO2+2e-=Mn5O102- |
| C、每生成1mol AgCl转移2mol电子 |
| D、Cl-不断向“水”电池的正极移动 |
下列叙述中正确的是( )
| A、电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
| B、向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
| C、常温下,将pH=10的氨水稀释,溶液中所有离子浓度都减小 |
| D、反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A、0.1mol?L-1NH4Cl溶液:c(NH4+)=c(Cl-) |
| B、0.1mol?L-1 Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为14.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的2倍.下列说法不正确的是( )
| A、X的氢化物溶液与其最高价氧化物对应的水化物溶液的酸碱性相反 |
| B、Y的氧化物既可与强酸反应又可与强碱反应,并可用来制作耐火材料 |
| C、X和Z的最高价氧化物对应的水化物的浓溶液都是具有强氧化性的酸 |
| D、Z的氢化物比X的氢化物更稳定 |
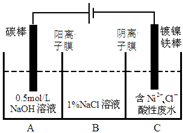 工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是( )已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是( )已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
| A、碳棒上发生的电极反应:4OH--4e-═O2↑+2H2O |
| B、电解过程中,B中NaCl溶液的物质的量浓度将不断减少 |
| C、为了提高Ni的产率,电解过程中需要控制废水pH |
| D、若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变 |