题目内容
7.由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaOH反应的有( )①-OH ②-CH3 ③-COOH ④
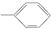 ⑤-CHO.
⑤-CHO.| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
分析 能与NaOH反应的有机物含-COOH、-COOC-、酚-OH,以此来解答.
解答 解:③-COOH分别与②④⑤组合的三种有机物均含-COOH,均与NaOH反应;
①与④组合成苯酚具有弱酸性,与NaOH反应;
①与⑤组合成HCOOH,与NaOH反应,
综上所述,共5种有机物能与NaOH反应,
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团及性质的关系为解答的关键,侧重分析与应用能力的考查,注意①③组合成碳酸为无机物,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
18.下列仪器中没有“0”刻度线的是( )
| A. | 托盘天平的游码刻度尺 | B. | 温度计 | ||
| C. | 酸式滴定管 | D. | 量筒 |
15.某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录(按编号填写):
实验结论:
Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:A E F.(多选)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录(按编号填写):
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | ① | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | / | Zn+Fe2+=Zn2++Fe | ② |
| ③ | 在FeCl3溶液中加入足量铁粉 | ③ | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ④ | ④ | / | / | Fe3+具有氧化性 |
Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:A E F.(多选)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
12.用NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 12.0g熔融的NaHSO4中含有的阳离子数为0.1NA | |
| B. | 2mol SO2和1mol O2在一定条件下充分反应后,所得混合气体的分子数大于2NA | |
| C. | 常温下,5.6g Fe片投入到足量的浓硝酸中,转移电子数为0.3NA | |
| D. | 常温常压下,14g乙烯和丙烯的混合气体中含有的原子总数为3NA |
19.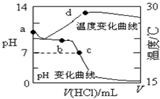 室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
 室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A. | a点由水电离出的c(H+)=1.0×10-14mol/L | |
| B. | b点时c(NH4+)+c(NH3•H2O)=c(Cl-) | |
| C. | c点时消耗的盐酸体积:V(HCl)<20.00mL | |
| D. | d点后,溶液温度略下降的主要原因是NH3•H2O电离吸热 |
16.下列叙述正确的是( )
| A. | 最高价含氧酸的酸性最强的元素位于周期表的最右上方 | |
| B. | 所有主族元素的最高正化合价等于它的族序数 | |
| C. | X的含氧酸的酸性比Y的含氧酸的酸性强,则非金属性X>Y | |
| D. | 离子化合物熔融状态都能导电 |
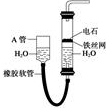 用图中的实验装置制取乙炔.
用图中的实验装置制取乙炔.