题目内容
15.乙醇(C2H5OH)和二甲醚(CH3OCH3)互为同分异构体物.且二甲醚不与钠反应,仅含碳、氢、氧三种元素的某化合物,其相对分子质量小于100,其中氧的质量分数为18.18%,已知该化合物不能与钠反应,该化合物的结构共有(不考虑立体异构)| A. | 5种 | B. | 6种 | C. | 8种 | D. | 10种 |
分析 仅含碳、氢、氧三种元素的某化合物,其相对分子质量为88,且氧的质量分数为18.18%,分子中N(O)=$\frac{88×18.18%}{16}$=1,去掉1个O原子后剩余基团总式量为88-16=72,则最大碳原子数目=$\frac{72}{12}$=6,则该有机物含有5个C原子、12H原子,分子式为C5H12O,该化合物不与钠反应,不含醇羟基,属于醚,再根据烃基异构进行分析解答.
解答 解:仅含碳、氢、氧三种元素的某化合物,其相对分子质量为88,且氧的质量分数为18.18%,分子中N(O)=$\frac{88×18.18%}{16}$=1,去掉1个O原子后剩余基团总式量为88-16=72,则最大碳原子数目=$\frac{72}{12}$=6,则该有机物含有5个C原子、12H原子,分子式为C5H12O,该化合物不与钠反应,不含醇羟基,属于醚,
当一个烃基为-CH3、另外烃基为-CH2CH2CH2CH3,-CH(CH3)CH2CH3,-C(CH3)3,-CH2CH(CH3)2,
当一个烃基为-CH2CH3,另外烃基为-CH2CH2CH3,-CH(CH3)2,
故符合条件的同分异构体共有6种,
故选B.
点评 本题考查有机物推断、同分异构体书写,侧重考查学生分析计算能力,注意利用残余法、商余法确定有机物分子式,同分异构体判断中可以利用形成醚的醇分析,难度中等.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
6.下列各组顺序的排列不正确的是( )
| A. | 熔点:Li>Na>K | B. | 还原性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H2SO4 | D. | 原子半径:Na<Mg<Al |
3.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入KSCN溶液,若溶液变成血红色,则一定有Fe3+ | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
10.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2 NA | |
| B. | 2.24LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| C. | 78g苯含有C=C双键的数目为3NA | |
| D. | 5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
20.FeCl2是一种常用的还原剂,实验室可以用多种方法来制备无水FeCl2.
I.按如图1装置用H2还原无水FeCl2制取.
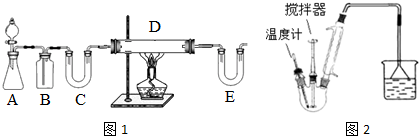
(1)装置C的作用是干燥氢气;E中盛放的试剂是碱石灰;D中反应的化学方程式为H2+2FeCl3$\frac{\underline{\;加热\;}}{\;}$2FeCl2+2HCl.
(2)若温度控制不当,产品中会含单质铁.检验产品中是否含铁的方案是取样,加入盐酸中,观察是否有气泡产生.
Ⅱ.按图2装置,在三颈烧瓶中放入162.5g无水氯化铁和225g氯苯,控制反应温度在128~139℃加热3h,反应接近100%.冷却,分离提纯得到粗产品.相关反应为2FeCl3+C6H5Cl→FeCl2+C6H4Cl2+HCl.有关数据如下:
(3)该制取反应中,作还原剂的是C6H5Cl.
(4)反应温度接近或超过C6H5Cl的沸点,但实验过程中C6H5Cl并不会大量损失.原因是实验使用了冷凝回流装置.
(5)冷却实验装置,将三颈瓶内物质经过过滤,洗涤沉淀并干燥后,得到粗产品.
①洗涤所用的试剂可以是苯;
②回收滤液中C6H5Cl的方案是蒸馏滤液,并收集132℃馏分.
(6)仅通过烧杯中的现象变化就可以监控氯化铁的转化率.若要监控氯化铁转化率已达到或超过90%,则烧杯中加入的试剂可以是滴有酚酞且含18gNaOH的溶液.
I.按如图1装置用H2还原无水FeCl2制取.

(1)装置C的作用是干燥氢气;E中盛放的试剂是碱石灰;D中反应的化学方程式为H2+2FeCl3$\frac{\underline{\;加热\;}}{\;}$2FeCl2+2HCl.
(2)若温度控制不当,产品中会含单质铁.检验产品中是否含铁的方案是取样,加入盐酸中,观察是否有气泡产生.
Ⅱ.按图2装置,在三颈烧瓶中放入162.5g无水氯化铁和225g氯苯,控制反应温度在128~139℃加热3h,反应接近100%.冷却,分离提纯得到粗产品.相关反应为2FeCl3+C6H5Cl→FeCl2+C6H4Cl2+HCl.有关数据如下:
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
(4)反应温度接近或超过C6H5Cl的沸点,但实验过程中C6H5Cl并不会大量损失.原因是实验使用了冷凝回流装置.
(5)冷却实验装置,将三颈瓶内物质经过过滤,洗涤沉淀并干燥后,得到粗产品.
①洗涤所用的试剂可以是苯;
②回收滤液中C6H5Cl的方案是蒸馏滤液,并收集132℃馏分.
(6)仅通过烧杯中的现象变化就可以监控氯化铁的转化率.若要监控氯化铁转化率已达到或超过90%,则烧杯中加入的试剂可以是滴有酚酞且含18gNaOH的溶液.
7.下列说法正确的是( )
| A. | 为了防止中秋月饼的富脂食物因被氧化而变质,常在包装袋里放还原铁粉 | |
| B. | 天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点 | |
| C. | 麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖 | |
| D. | 若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
5.下列离子方程式书写正确的是( )
| A. | 用铜电极电解硝酸银溶液:4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+ | |
| B. | FeS中加入足量稀硝酸:FeS+2 H+=Fe2++H2↑ | |
| C. | 石灰石溶于醋酸溶液中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | 澄清石灰水中通入过量的CO2:CO2+OH-=HCO3- |
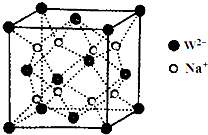 前四周期元素X、Y、Z、W、R、Q的原子序数依次增大,X的核外电子总数与其周期数相同;Y有三个能级,且每个能级上的电子数相等;Z原子单电子数在同周期元素中最多;W与Z同周期,第一电离能比Z的低;R与Y同一主族,Q的最外层电子数为2,其他电子层电子均处于饱和状态.请回答下列问题:
前四周期元素X、Y、Z、W、R、Q的原子序数依次增大,X的核外电子总数与其周期数相同;Y有三个能级,且每个能级上的电子数相等;Z原子单电子数在同周期元素中最多;W与Z同周期,第一电离能比Z的低;R与Y同一主族,Q的最外层电子数为2,其他电子层电子均处于饱和状态.请回答下列问题: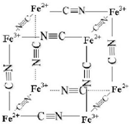 铁及其化合物在生产生活及科学研究方面应用非常广泛.
铁及其化合物在生产生活及科学研究方面应用非常广泛. ,其空间构型为直线型.
,其空间构型为直线型.