题目内容
下列反应的离子方程式,正确的是( )
A、少量NaHSO4溶液与Ba(OH)2溶液混合:S
| ||
| B、醋酸除水垢:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O | ||
| C、漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | ||
| D、少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.NaHSO4完全反应,生成硫酸钡、水、NaOH;
B.碳酸钙、醋酸、水、二氧化碳在离子反应中均保留化学式,反应生成醋酸钙、水、二氧化碳;
C.过量二氧化碳,反应生成碳酸氢钙和HClO;
D.电子、电荷不守恒.
B.碳酸钙、醋酸、水、二氧化碳在离子反应中均保留化学式,反应生成醋酸钙、水、二氧化碳;
C.过量二氧化碳,反应生成碳酸氢钙和HClO;
D.电子、电荷不守恒.
解答:
解:少量NaHSO4溶液与Ba(OH)2溶液混合的离子反应为Ba2++SO42-+H++OH-═BaSO4↓+H2O,故A错误;
B.醋酸除水垢的离子反应为CaCO3↓+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O,故B正确;
C.漂白粉溶液中通入过量的CO2的离子反应为ClO-+H2O+CO2═HCO3-+HClO,故C错误;
D.少量金属钠放入冷水中的离子反应为2Na+2H2O═2OH-+2Na++H2↑,故D错误;
故选B.
B.醋酸除水垢的离子反应为CaCO3↓+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O,故B正确;
C.漂白粉溶液中通入过量的CO2的离子反应为ClO-+H2O+CO2═HCO3-+HClO,故C错误;
D.少量金属钠放入冷水中的离子反应为2Na+2H2O═2OH-+2Na++H2↑,故D错误;
故选B.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的化学反应及离子反应的书写方法解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,注意选项C为解答的易错点,题目难度不大.

练习册系列答案
相关题目
下列反应中,离子方程式正确的是( )
| A、大理石溶于盐酸中:CO32-+2H+=CO2↑+H2O |
| B、AlCl3溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、硫酸镁溶液与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓ |
| D、氯化铁溶液中加入铜片:Fe3++Cu=Fe2++Cu2+ |
下列离子组能在水溶液中大量共存的是( )
| A、Mg2+、Fe3+、SO42-、I- |
| B、Fe2+、H+、Cl-、NO3- |
| C、Na+、Al3+、AlO2-、Cl- |
| D、Mg2+、Fe2+、SO42-、Cl- |
用下列有关实验装置进行相应实验,能达到实验目的是( )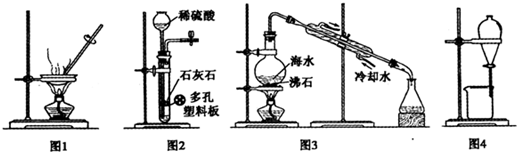

| A、用图1装置蒸干CuCl2饱和溶液制备CuCl2晶体 |
| B、用图2装置制取二氧化碳气体 |
| C、用图3装置蒸馏海水制取少量淡水 |
| D、用图4装置分离乙醇与乙酸乙酯的混合物 |
下列浓度关系正确的是( )
| A、0.1mol/L的NH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+) |
| B、0.1mol/L的KOH溶液中通入标准状况下的CO2气体3.36L,所得溶液中:c(K+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C、0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,所得溶液呈碱性:c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+) |
| D、pH相同的NaOH溶液、CH3COONa溶液、Na2CO3溶液、NaHCO3溶液的浓度:c(NaOH)<c(CH3COONa)<c(NaHCO3)<c(Na2CO3) |
 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO4-+5C2O42-+16H+
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO4-+5C2O42-+16H+ 如图,外接电源为Zn-MnO2干电池,甲乙为相互串联的两个电解池,请回答:
如图,外接电源为Zn-MnO2干电池,甲乙为相互串联的两个电解池,请回答: 邻羟基苯甲酸(俗名水杨酸)其结构简式如图所示:
邻羟基苯甲酸(俗名水杨酸)其结构简式如图所示: