题目内容
2.T℃时,N2与H2反应生成NH3,其能量变化如图(Ⅰ)所示.若保持其他条件不变,温度分别为T1℃和T2℃时,H2的体积分数与时间的关系如图(Ⅱ)所示.则下列结论不正确的是( )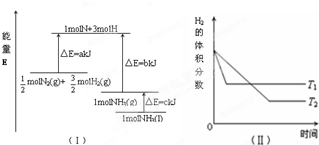
| A. | 该反应的热化学方程式:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=-(b-a)kJ•mol-1 | |
| B. | 该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1 | |
| C. | T1>T2,且正反应为放热反应 | |
| D. | 其他条件不变,升高温度,正、逆反应速率均增大,且H2的转化率增大 |
分析 A.由图可知,$\frac{1}{2}$molN2(g)与$\frac{3}{2}$molH2(g)反应生成1molNH3(g),放出(b-a)kJ的热量;
B.由图可知,$\frac{1}{2}$molN2(g)与$\frac{3}{2}$molH2(g)反应生成1molNH3(l),放出(b+c-a)kJ的热量;
C.由图II可知,T1先达到平衡,且T1时氢气的体积分数大,可知升高温度平衡逆向移动;
D.升高温度,平衡逆向移动.
解答 解:A.由图可知,$\frac{1}{2}$molN2(g)与$\frac{3}{2}$molH2(g)反应生成1molNH3(g),放出(b-a)kJ的热量,则热化学方程式为$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=-(b-a)kJ•mol-1,故A正确;
B.由图可知,$\frac{1}{2}$molN2(g)与$\frac{3}{2}$molH2(g)反应生成1molNH3(l),放出(b+c-a)kJ的热量,则热化学方程式为N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1,故B正确;
C.由图II可知,T1先达到平衡,且T1时氢气的体积分数大,可知升高温度平衡逆向移动,则T1>T2,且正反应为放热反应,故C正确;
D.该反应为放热反应,升高温度,正、逆反应速率均增大,平衡逆向移动,H2的转化率减小,故D错误;
故选D.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、平衡移动为解答的关键,侧重分析与应用能力的考查,注意图象分析,题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
12.在某溶液M中加入物质X,物理量y与物质X体积的关系如图所示,下列有关溶液M、物质X和物理量y的推断合理的是( )


| 选项 | 溶液M | 物质X | 物理量y |
| A | 含Mg2+、Al3+、NH4+的溶液 | KOH溶液 | 沉淀的物质的量 |
| B | 含CO32-、HCO3-的溶液 | 盐酸 | 二氧化碳的体积 |
| C | 含OH-、AlO2-、SiO3 2-、CO32-的溶液 | NaHSO4溶液 | 沉淀的质量 |
| D | 含Ba(OH)2、NaOH、NaAlO2的溶液 | CO2 | 沉淀的物质的量 |
| A. | A | B. | B | C. | C | D. | D |
13.硝酸与金属反应往往产生氮氧化物,但是在某些特殊情况则不然.将稀硝酸(HNO3浓度低于2mol•L一1)与过量金属镁缓和反应放出一种无色无毒气体A,反应完全后向剩余溶液中加人过量NaOH固体并加热,放出气体B,将两次放出气体全部收集并混合,用碱石灰干燥后缓慢通过足量的灼热氧化铜固体,观察到固体变红,将剩余气体用浓硫酸干燥,最后气体体积变为原来的四分之三,则下列分析正确的是(本题中所有气体体积均为相同条件下测得的体积)( )
| A. | 无色无毒气体A为H2 | |
| B. | 最后气体为NH3 | |
| C. | 在镁与硝酸反应过程中还原剂与氧化剂的物质的量之比为5:1 | |
| D. | 气体A与气体B的体积比为1:1 |
10.下列酸溶液的pH相同时,其物质的量浓度最小的是( )
| A. | H2S | B. | H2SO4 | C. | HClO | D. | HNO3 |
17.已知:将a mol Cl2通入含b mol NaOH的溶液中两者恰好完全反应,产物中可能有NaCl、NaClO、NaClO3.温度不同,三者的量也不同.下列说法不正确的是( )
| A. | 改变温度,当产物中NaClO3的物质的量最大时,发生的离子反应为:3Cl2+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$5Cl-+ClO3-+3H2O | |
| B. | 某温度下,反应后若溶液中c(ClO-):c(ClO3-)=1:2,发生的离子反应为:7Cl2+14OH-$\frac{\underline{\;\;△\;\;}}{\;}$11Cl-+ClO-+2ClO3-+7H2O | |
| C. | 参加反应的Cl2与NaOH的物质的量的关系一定是a=0.5b | |
| D. | 改变温度,反应中转移电子的物质的量可能为b mol |
14.下列溶液中,加热后颜色一定变浅的是( )
| A. | 稀氨水和酚酞溶液 | B. | 溶有SO2的品红溶液 | ||
| C. | 滴有酚酞的氢氧化钙溶液 | D. | 滴有酚酞的Na2CO3溶液 |
11.下列说法正确的是( )
| A. | 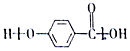 的结构中含有酯基 的结构中含有酯基 | |
| B. | 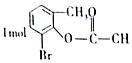 一定条件下与足量NaOH溶液反应,最多消耗3molNaOH 一定条件下与足量NaOH溶液反应,最多消耗3molNaOH | |
| C. | 按系统命名法,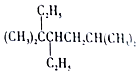 的名称为3,3,6-三甲基-4-乙基庚烷 的名称为3,3,6-三甲基-4-乙基庚烷 | |
| D. | 油脂和蛋白质都是能发生水解反应的高分子化合物 |