题目内容
家用液化气中的主要成分之一是丁烷(C4H10).已知1mol液态水汽化时需要吸收44KJ热量.
(1)当58Kg丁烷完全燃烧生成CO2和液态水时,放出的热量是3×106 KJ,求1mol丁烷完全燃烧产生液态水时放出的热量为多少KJ?
(2)求1mol丁烷完全燃烧产生水蒸汽时放出的热量为多少KJ?
(1)当58Kg丁烷完全燃烧生成CO2和液态水时,放出的热量是3×106 KJ,求1mol丁烷完全燃烧产生液态水时放出的热量为多少KJ?
(2)求1mol丁烷完全燃烧产生水蒸汽时放出的热量为多少KJ?
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:(1)化学反应的热效应和反应物的物质的量之间成正比例关系;
(2)根据(1)计算出的1mol丁烷完全燃烧产生液态水时放出的热量结合1mol液态水汽化时需要吸收44kJ热量来回答计算.
(2)根据(1)计算出的1mol丁烷完全燃烧产生液态水时放出的热量结合1mol液态水汽化时需要吸收44kJ热量来回答计算.
解答:
解:(1)58kg即1000mol丁烷完全燃烧生成CO2和液态水时,放出的热量是3×106 kJ,所以1mol丁烷完全燃烧产生液态水时放出的热量为3×103kJ,
答:1mol丁烷完全燃烧产生液态水时放出的热量为3×103kJ;
(2)1mol丁烷完全燃烧产生液态水时放出的热量为3×103kJ,1mol液态水汽化时需要吸收44kJ的热量,所以1mol丁烷完全燃烧产生水蒸汽时放出的热量为3×103kJ-44kJ=2956kJ.答:1mol丁烷完全燃烧产生水蒸汽时放出的热量为2956kJ.
答:1mol丁烷完全燃烧产生液态水时放出的热量为3×103kJ;
(2)1mol丁烷完全燃烧产生液态水时放出的热量为3×103kJ,1mol液态水汽化时需要吸收44kJ的热量,所以1mol丁烷完全燃烧产生水蒸汽时放出的热量为3×103kJ-44kJ=2956kJ.答:1mol丁烷完全燃烧产生水蒸汽时放出的热量为2956kJ.
点评:本题考查学生化学反应的热效应和反应物的物质的量之间的关系知识,注意知识的归纳和梳理关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
A、B、C均为中学常见的单质或化合物,一定条件下,存在转化关系:A+H2O→B+C.下列说法正确的是( )
| A、若B为强碱,则A一定为金属钠 |
| B、若B为强酸,则A一定为氯气 |
| C、若C为H2,则H2O一定作氧化剂 |
| D、若C为O2,则H2O一定作还原剂 |
 室温下,在0.2mol?L-1 Al2(SO4)3溶液中,逐滴加入1.0mol?L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正确的是( )
室温下,在0.2mol?L-1 Al2(SO4)3溶液中,逐滴加入1.0mol?L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正确的是( )| A、a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3OH-?Al(OH)3 |
| B、a-b段,溶液pH增大,Al3+浓度不变 |
| C、b-c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| D、d点时,Al(OH)3沉淀开始溶解 |
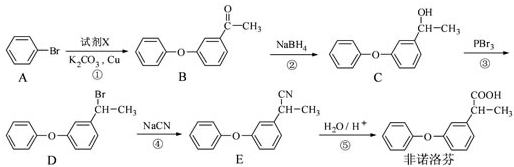
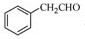 为原料制备
为原料制备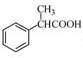 的合成路线流程图(无机试剂任用),合成路线路程图示例如下:
的合成路线流程图(无机试剂任用),合成路线路程图示例如下: