题目内容
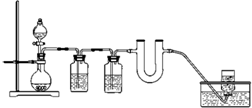 为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验.
为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验.(1)生成CO2的化学反应方程式:
(2)饱和碳酸氢钠溶液的作用是除去CO2中混有的HCl气体,浓H2SO4的作用是
(3)U形管中的现象是
考点:钠的重要化合物
专题:元素及其化合物
分析:(1)实验室用CaCO2和稀HCl制取CO2;
(2)浓硫酸具有吸水性;
(3)CO2和Na2O2反应生成白色固体Na2CO3,同时生成无色气体.
(2)浓硫酸具有吸水性;
(3)CO2和Na2O2反应生成白色固体Na2CO3,同时生成无色气体.
解答:
解:(1)实验室用CaCO2和稀HCl制取CO2,反应方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O,故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)浓硫酸具有吸水性,且和二氧化碳不反应,所以浓硫酸作干燥剂,故答案为:作干燥剂;
(3)CO2和Na2O2反应生成白色固体Na2CO3,同时生成无色气体,所以看到的现象是固体由淡黄色变为白色,反应方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案为:淡黄色固体变为白色;2Na2O2+2CO2=2Na2CO3+O2.
(2)浓硫酸具有吸水性,且和二氧化碳不反应,所以浓硫酸作干燥剂,故答案为:作干燥剂;
(3)CO2和Na2O2反应生成白色固体Na2CO3,同时生成无色气体,所以看到的现象是固体由淡黄色变为白色,反应方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案为:淡黄色固体变为白色;2Na2O2+2CO2=2Na2CO3+O2.
点评:本题考查了探究过氧化钠和二氧化碳的反应,明确二氧化碳制取、过氧化钠和二氧化碳的反应原理即可解答,能从整体上分析装置中各个仪器的作用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
化学与数学有着密切的关系,将某些化学知识用数轴表示,可以收到直观形象、简明易记的效果.下列用数轴表示的化学知识中正确的是( )
A、常温条件下,酚酞的变色范围: |
B、分散系的分类: |
C、HCl和NaAlO2溶液反应后铝元素的存在形式: |
D、CO2通入澄清石灰水中反应的产物: |
通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似.有关NCl3分子的下列说法中正确的是( )
| A、是由极性键形成的非极性分子 |
| B、所有N-Cl键的键长均相等 |
| C、Cl-N-Cl的键角是120° |
| D、比NF3键能更大,更稳定 |
下列反应的离子方程式正确的是( )
| A、铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B、钠加入到足量的水中:Na+2H2O=Na++2OH-+H2↑ |
| C、AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ |
| D、金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ |
在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(SO2)随时间的变化如表:则下列说法正确的是( )
| 时间/min | 0 | 1 | 2 | 3 | 4 | 3 |
| n(SO2)/mol | 0.20 | 0.1 6 | 0.13 | 0.11 | 0.08 | 0.08 |
| A、当v(SO2)=v(SO3)时,说明该反应已达到平衡状态 |
| B、平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大 |
| C、若升高温度,则SO2的反应速率会变大,平衡常数K值会增大 |
| D、用O2表示0~4min内该反应的平均速率为0.005mol/(L?min) |
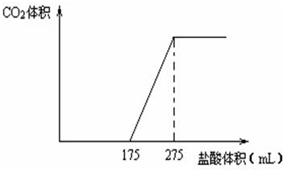 取NaHCO3和Na2O2的固体混合物x g放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如下图所示.试回答下列问题:
取NaHCO3和Na2O2的固体混合物x g放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如下图所示.试回答下列问题: