题目内容
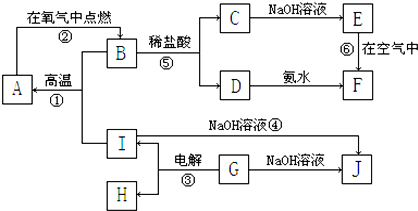
 如图表示A~E五种物质的相互转化关系,其中A为淡黄色粉末,C为单质,D为离子化合物.
如图表示A~E五种物质的相互转化关系,其中A为淡黄色粉末,C为单质,D为离子化合物.(1)推断A为
(2)写出相关方程式:
③化学方程式
(3)请写出过量的E和Ca(HCO3)2溶液反应的离子方程式:
考点:无机物的推断
专题:推断题
分析:A为淡黄色粉末,能和CO2、H2O反应,则A是Na2O2,B是Na2CO3、E是NaOH,C为单质,C能和水反应,且可以反应得到过氧化钠,则C是Na,C和氯气反应生成D是NaCl,氢氧化钠与盐酸反应得到氯化钠,氢氧化钠与二氧化碳反应得到碳酸钠,碳酸钠与盐酸等反应可以得到氯化钠,据此解答.
解答:
解:A为淡黄色粉末,能和CO2、H2O反应,则A是Na2O2,B是Na2CO3、E是NaOH,C为单质,C能和水反应,且可以反应得到过氧化钠,则C是Na,C和氯气反应生成D是NaCl,氢氧化钠与盐酸反应得到氯化钠,氢氧化钠与二氧化碳反应得到碳酸钠,碳酸钠与盐酸等反应可以得到氯化钠,
(1)通过以上分析知,A是Na2O2、B是Na2CO3、C是Na、D是NaCl,
故答案为:Na2O2;Na2CO3;Na;NaCl;
(2)反应③是过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应方程式为:2Na2O2+2CO2═2Na2CO3+O2;
反应⑧是钠和水反应生成氢氧化钠和氢气,反应离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;2Na+2H2O═2Na++2OH-+H2↑;
(3)过量的NaOH溶液和碳酸氢钙溶液反应生成碳酸钙、碳酸钠和水,离子方程式为:2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O,
故答案为:2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O.
(1)通过以上分析知,A是Na2O2、B是Na2CO3、C是Na、D是NaCl,
故答案为:Na2O2;Na2CO3;Na;NaCl;
(2)反应③是过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应方程式为:2Na2O2+2CO2═2Na2CO3+O2;
反应⑧是钠和水反应生成氢氧化钠和氢气,反应离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;2Na+2H2O═2Na++2OH-+H2↑;
(3)过量的NaOH溶液和碳酸氢钙溶液反应生成碳酸钙、碳酸钠和水,离子方程式为:2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O,
故答案为:2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O.
点评:本题考查无机物推断,涉及钠元素单质化合物性质,以A的颜色及发生的反应为突破口采用正逆结合的方法进行推断,明确物质的性质是解本题关键,(3)中离子方程式的书写是难点、易错点,注意该反应量不同产物不同,题目难度中等.

练习册系列答案
相关题目
阿司匹林是常见的解热镇痛药,结构简式如图 所示,有关阿司匹林的说法正确的是( )
所示,有关阿司匹林的说法正确的是( )
 所示,有关阿司匹林的说法正确的是( )
所示,有关阿司匹林的说法正确的是( )| A、能发生取代、酯化反应,但不能发生氧化、还原反应 |
| B、1mol该物质完全氧化最多可消耗10mol氧气 |
| C、1mol该物质最多可与3mol NaOH发生反应 |
| D、阿司匹林分子中最多可以有13个原子在同一平面上 |
下列离子方程式书写正确的是( )
| A、银投入硝酸铜溶液中:Cu2++2Ag=Cu+2Ag+ |
| B、漂白粉溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| C、澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
| D、向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
若NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,2.24L四氯化碳含碳原子数为0.1NA | ||
B、标准状况下,a L的氧气和氮气的混合物含有的分子数为
| ||
| C、7g CnH2n中含有的氢原子数为2NA | ||
| D、2L1mol/L的盐酸中所含氯化氢分子数为2NA |
下列各组物质中无论是反应条件的不同,还是试剂用量的不同,都能用同一个化学方程式表示的是( )
| A、金属钠,氧气 |
| B、Cu,FeCl3溶液 |
| C、Fe,HNO3溶液 |
| D、浓氨水,AgNO3溶液 |
 如图所示中各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C和D为无色气体,C能使湿润的红色石蕊试纸变蓝,X分解产生A、B和C三种产物的比值为1:1:1.
如图所示中各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C和D为无色气体,C能使湿润的红色石蕊试纸变蓝,X分解产生A、B和C三种产物的比值为1:1:1.