题目内容
12.下列有关实验原理、装置、操作或结论的描述中,正确的(或实验能达到预期目的)有(有关装置中的夹持仪器略去未画)( )项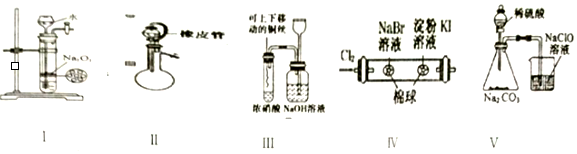
Ⅰ仿启普发生器制少量氧气Ⅱ.该装置检查气密性(止水夹已关)一打开分液漏斗活塞,液体顺利流下
Ⅲ进行铜与浓硝酸反应的实验Ⅳ.证明氧化性Cl2>Br2>I2Ⅴ.验证酸性的强弱,H2SO4>H2CO3>HClO.
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
分析 Ⅰ.过氧化钠为粉末固体,隔板不能使固体与液体分离;
Ⅱ.该装置中用橡皮管连接蒸馏烧瓶和分液漏斗,大气压相等,无法检验装置的气密性;
Ⅲ.浓硝酸和铜反应生成二氧化氮,用氢氧化钠溶液吸收;
Ⅳ.生成的溴中含有氯气,不能排除氯气的干扰;
Ⅴ.烧杯中二氧化碳与次氯酸钠的反应没有明显现象,无法判断是否反应.
解答 解:Ⅰ.过氧化钠为粉末固体,隔板不能使固体与液体分离,则图中装置不能用于制备少量氧气,故Ⅰ错误;
Ⅱ.橡胶管上下连通,无法检验该装置的气密性,故Ⅱ错误;
Ⅲ.浓硝酸和铜反应生成二氧化氮,可用氢氧化钠溶液吸收,防止污染空气,故Ⅲ正确;
Ⅳ.生成的溴中含有氯气,不能排除氯气的干扰,故Ⅳ错误;
Ⅴ.碳酸与次氯酸钠反应生成次氯酸和碳酸氢钠,该反应没有明显现象,则无法判断二者发生了反应,则无法证明酸性H2CO3>HClO,故Ⅴ错误;
根据分析可知,正确的只有1个,
故选A.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及气体制备、装置气密性检验、酸性、氧化性强弱比较等知识,明确常见化学实验基本操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
2.近年来“雾霾”污染日益严重,原因之一是机动车尾气中含有NO、NO2、CO等气体,火力发电厂释放出大量的NOx、SO2和CO2等气体也是其原因,现在对其中的一些气体进行了一定的研究:
(1)用 CH4催化还原氮氧化物可以消除氮氧化物的污染.
已知:①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574 kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160 kJ/mol
③H2O(g)═H2O(l)△H=-44.0 kJ/mol
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式:2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O(l)△H=-1910kJ/mol.
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=akJ•mol-1.
在T1℃时,反应进行到不同时间测得各物质的浓度如表:
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率V(NO)=0.042mol•L-1•min-1;计算该反应的平衡常数K=;
②30min后,只改变某一条件,根据上表中的数据判断改变的条件可能是BE(填字母编号).
A.通人一定量的CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通人一定量的NO E.加入一定量的活性炭
③若50min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:1:1,则达到新平衡时NO的转化率降低(填“升高”或“降低”),a< 0(填“>”或“<”).
(1)用 CH4催化还原氮氧化物可以消除氮氧化物的污染.
已知:①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574 kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160 kJ/mol
③H2O(g)═H2O(l)△H=-44.0 kJ/mol
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式:2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O(l)△H=-1910kJ/mol.
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=akJ•mol-1.
在T1℃时,反应进行到不同时间测得各物质的浓度如表:
 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
②30min后,只改变某一条件,根据上表中的数据判断改变的条件可能是BE(填字母编号).
A.通人一定量的CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通人一定量的NO E.加入一定量的活性炭
③若50min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:1:1,则达到新平衡时NO的转化率降低(填“升高”或“降低”),a< 0(填“>”或“<”).
3.下列事实能用勒夏特列原理解释的是( )
| A. | 对由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色加深 | |
| B. | 使用铁作催化剂,使N2和H2在一定条件下合成为NH3 | |
| C. | 可用排饱和食盐水法收集氯气 | |
| D. | 500℃时比室温更有利于合成氨的反应(已知合成氨的反应时放热反应) |
17.下列分类方法中正确的是( )
| A. | 根据物质能否导电,可以将化合物分为电解质和非电解质 | |
| B. | 根据氧化物中是否含有金属元素,可以将氧化物分为碱性氧化物和酸性氧化物 | |
| C. | 根据组成元素的种类,将纯净物分为单质和化合物 | |
| D. | 根据分散系的稳定性大小,可以将分散系分为胶体、浊液和溶液 |
4.现有下列十种物质:①O2 ②Fe ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧硫酸钠溶液 ⑨稀硝酸 ⑩Cu2(OH)2CO3.
(1)按物质的树状分类法填写表格的空白处:
(2)上述物质中属于非电解质的有④;上述物质中能与盐酸反应的电解质有③⑥⑩(填序号).
(1)按物质的树状分类法填写表格的空白处:
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 |
| 属于该类的物质 | ② | ⑧⑨ |
15.二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向.
(1).用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H,在T1℃时,反应进行到不同时间测得各物质的量浓度如表:
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率
v(N2)=0.03mol•L-1•min-1;计算该反应的平衡常数K=0.5625.
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是BC(填字母代号).
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率降低(填“升高”或“降低”),△H<0(填“>”或“<”).
(2)工业上用CO2和H2反应合成二甲醚.已知:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-49.1kJ•mol-1
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24.5kJ•mol-1
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H=-122.7kJ•mol-1.
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:CH3OCH3-12e-+16OH-═2CO32-+11H2O.
(1).用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H,在T1℃时,反应进行到不同时间测得各物质的量浓度如表:
| 时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.96 | 0.96 |
| N2 | 0 | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
| CO2 | 0 | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
v(N2)=0.03mol•L-1•min-1;计算该反应的平衡常数K=0.5625.
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是BC(填字母代号).
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率降低(填“升高”或“降低”),△H<0(填“>”或“<”).
(2)工业上用CO2和H2反应合成二甲醚.已知:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-49.1kJ•mol-1
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24.5kJ•mol-1
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H=-122.7kJ•mol-1.
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:CH3OCH3-12e-+16OH-═2CO32-+11H2O.