题目内容
15.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.(1)氮、磷、砷的电负性的大小关系是N>P>As,砷原子M层电子排布式为3s23p63d10.
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是
Fe3+提供空轨道,CN-提供孤电子形成配位键.
(3)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,沸点高低的原因是CH4和SiH4比较,影响熔沸点的因素是分子间作用力,SiH4之间的分子间作用力大,熔沸点高.
②NH3和PH3比较,分解温度高低的原因是NH3和PH3比较,影响分解温度的因素是共价键的强弱,N原子的半径比P原子的半径小,共价键的键长短,供价键强,分解温度高.
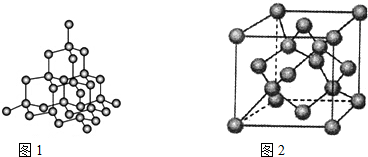
(4)金刚石是原子晶体,含有的最小环是六元环(如图2),每个碳原子连接12个六元环,如图1是金刚石的晶胞,若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,碳原子在晶胞中的空间占有率$\frac{32π{r}^{3}}{3{a}^{3}}$×100%(不要求计算过程).
分析 (1)同主族自上而下电负性减小;As原子处于的第四周期VA族,M层各能级均填充满;
(2)Fe3+提供空轨道,CN-提供孤电子形成配位键;
(3)①影响CH4和SiH4熔沸点的因素是分子间作用力,相对分子质量越大,分子间作用力越强,熔沸点越高;
②影响NH3和PH3分解温度的因素是共价键的强弱,键长短,供价键强,分解温度高;
(4)在金刚石晶体中,C原子所连接的最小环为六元环,每个C原子连接4个碳原子,连接的4个C原子中每个C原子形成3个六元环;
根据均摊法计算晶胞中碳原子数目,再计算晶胞中碳原子总体积、晶胞体积,碳原子在晶胞中的空间占有率=$\frac{晶胞中碳原子总体积}{晶胞体积}$×100%.
解答 解:(1)同主族自上而下电负性减小,故电负性N>P>As;As原子处于的第四周期VA族,M层各能级均填充满,M层电子排布式为:3s23p63d10,
故答案为:N>P>As; 3s23p63d10;
(2)Fe3+提供空轨道,CN-提供孤电子,Fe3+与CN-之间形成配位键,
故答案为:配位键;
(3)①CH4和SiH4比较,影响熔沸点的因素是分子间作用力,SiH4之间的分子间作用力大,熔沸点高,
故答案为:CH4和SiH4比较,影响熔沸点的因素是分子间作用力,SiH4之间的分子间作用力大,熔沸点高;
②NH3和PH3比较,影响分解温度的因素是共价键的强弱,N原子的半径比P原子的半径小,共价键的键长短,供价键强,分解温度高,
故答案为:NH3和PH3比较,影响分解温度的因素是共价键的强弱,N原子的半径比P原子的半径小,共价键的键长短,供价键强,分解温度高;
(4)在金刚石晶体中,C原子所连接的最小环为六元环,每个C原子连接4个碳原子,连接的4个C原子中每个C原子形成3个六元环,所以金刚石晶体中每个C原子能形成12个六元环;
晶胞中碳原子数目=4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,晶胞中碳原子总体积=8×$\frac{4}{3}$πr3,晶胞体积为a3,碳原子在晶胞中的空间占有率=$\frac{8×\frac{4}{3}π{r}^{3}}{{a}^{3}}$×100%=$\frac{32π{r}^{3}}{3{a}^{3}}$×100%,
故答案为:12;$\frac{32π{r}^{3}}{3{a}^{3}}$×100%.
点评 本题是对物质结构与性质的考查,涉及晶胞结构与计算、电负性、核外电子排布、配合物、分子结构与性质等,(4)为易错点,注意理解识记中学常见晶胞计算.

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案| 选项 | 实验 | 试剂 | 操作方法 |
| A | 除去CH4中的C2H4 | 溴水 | 洗气 |
| B | 除去工业酒精中的水 | CaO | 蒸馏 |
| C | 除去苯中的溴 | 乙醇 | 分液 |
| D | 从肥皂、甘油的混合液中分离出肥皂 | NaCl | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 1mol•L-1NaCl溶液含有NA个Na+ | |
| B. | 1 L 0.1mol•L-1氨水含有0.1NA个OH- | |
| C. | 电解饱和食盐水若产生2g氢气,则转移2NA个电子 | |
| D. | 将0.1mol氯化铁溶于1 L水中,所得溶液含有0.1NA个Fe3+ |
| A. | 114号元素在周期表中第七周期第VIA族,属于金属元素 | |
| B. | 晶体硅熔点高硬度大,可用于制作光导纤维 | |
| C. | 光束通过下列分散系①有尘埃的空气②胆矾溶液③墨水④稀豆浆时,均产生丁达尔效应 | |
| D. | 为了除去MgCl2酸性溶液中的Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入MgCO3,过滤后,再向滤液中加入适量的盐酸 |
| A. | Ca2+、Na+、SO42-、MnO4- | B. | K+、Fe2+、SO42-、HCO3- | ||
| C. | Ba2+、K+、Al3+、Cl- | D. | Na+、Ba2+、Cl-、NO3- |
| A. | Al2(SO4)3与NaOH | B. | NaHSO4与Ba(OH)2 | C. | Na2CO3与HCl | D. | NaAlO2与H2SO4 |

 ⑥CH2=CHCH3和CH2=CH2;
⑥CH2=CHCH3和CH2=CH2;