题目内容
设C+CO2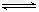 2CO-Q1(吸热反应)反应速率为 u1,N2+3H2
2CO-Q1(吸热反应)反应速率为 u1,N2+3H2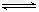 2NH3+Q2(放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为
2NH3+Q2(放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为
| A.同时增大 | B.同时减小 | C.增大,减小 | D.减小,增大 |
A
解析试题分析:只要升高温度,无论反应是吸热还是放热,反应速率都会增大,所以,只有A正确。故选A。
考点:影响化学反应速率的因素
点评:本题考查的是温度对化学平衡的影响,学生要熟记化学平衡的影响因素,温度,浓度,压强,接触面积,催化剂等对平衡的影响特点。在判断化学平衡的移动方向时,大多数都是根据勒下特列原理:化学平衡会向减弱这种改变的方向进行。这句话可能很难理解,你这样想:对于升高温度,化学平衡体系升温,而在升高温度之前的化学平衡体系的温度没有现在高,那么,既然外界环境对体系的改变是“升温”,那么根据勒下特列原理,化学平衡会向减弱(减弱“升温”)这种改变的方向进行,即化学平衡会向着吸热的方向进行,这样才能减弱升温给体系所带来的影响。同理,对于降低温度,反应会向着“能够减弱‘降低温度’”的方向进行,即向着放热的方向进行,只有这样才能够减弱“降低温度”对反应所带来的影响。

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
 2CO-Q1(吸热反应)反应速率为 u1,N2+3H2
2CO-Q1(吸热反应)反应速率为 u1,N2+3H2 2CO(正反应吸热),正反应的反应速率为v1;N2+3H2
2CO(正反应吸热),正反应的反应速率为v1;N2+3H2 2CO (吸热反应)反应速率为 u1,N2+3H2
2CO (吸热反应)反应速率为 u1,N2+3H2 2NH3 (放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为( )
2NH3 (放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为( )