题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、22.4 L O2中含有氧分子的个数为2NA |
| B、24g Mg与足量氧气反应转移的电子数为2NA |
| C、28g N2中含有氮原子的个数为NA |
| D、1L 1 mol?L-1MgCl2溶液中含有氯离子个数为NA |
考点:阿伏加德罗常数
专题:
分析:A、氧气所处的状态不明确;
B、根据镁的物质的量和与反应后的价态来分析;
C、根据氮气的物质的量和氮气是双原子分子来分析;
D、根据1molMgCl2中含2mol氯原子来分析.
B、根据镁的物质的量和与反应后的价态来分析;
C、根据氮气的物质的量和氮气是双原子分子来分析;
D、根据1molMgCl2中含2mol氯原子来分析.
解答:
解:A、氧气所处的状态不明确,不一定是标况,故22.4L氧气的物质的量不一定是1mol,故A错误;
B、24g镁的物质的量为1mol,反应后镁元素的价态为+2价,故1mol镁转移的电子为2mol,故B正确;
C、28g氮气的物质的量为1mol,而氮气是双原子分子,故1mol氮气中含2mol氮原子,故C错误;
D、1L1mol/LMgCl2溶液的物质的量为1mol,而1molMgCl2中含2mol氯原子,故D错误.
故选B.
B、24g镁的物质的量为1mol,反应后镁元素的价态为+2价,故1mol镁转移的电子为2mol,故B正确;
C、28g氮气的物质的量为1mol,而氮气是双原子分子,故1mol氮气中含2mol氮原子,故C错误;
D、1L1mol/LMgCl2溶液的物质的量为1mol,而1molMgCl2中含2mol氯原子,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
一定温度和压强下,30L 某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024个原子组成,下列有关说法中不正确的是( )
| A、该温度和压强可能是标准状况 |
| B、标准状况下该纯净物若为气态,其体积是22.4L |
| C、该气体分子为双原子分子 |
| D、若在该条件下O2为气态,则此时1mol O2的体积为30L |
下列每组反应一定能用同一离子方程式表示的是( )
| A、CaCO3、Na2CO3分别与盐酸反应 |
| B、CuO分别与稀硫酸、稀盐酸、稀硝酸反应 |
| C、H2SO4、K2SO4溶液分别与Ba(OH)2溶液反应 |
| D、Na分别与水、稀盐酸反应 |
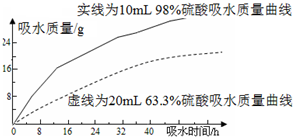 探究浓硫酸的吸水性.某同学把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,根据室温环境下实验的数据绘成的曲线如图.由如图曲线你能得到的实验结论有哪些?(写两点)
探究浓硫酸的吸水性.某同学把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,根据室温环境下实验的数据绘成的曲线如图.由如图曲线你能得到的实验结论有哪些?(写两点)