题目内容
将0.1mol的KCl和0.1mol的AlCl3溶于水配成100mL混合溶液,下列溶液中Cl-浓度与该溶液浓度相等的是( )
| A、3 mol?L-1 的NaCl溶液 |
| B、2mol?L-1 的FeCl3溶液 |
| C、2 mol?L-1 的MgCl2溶液 |
| D、2 mol?L-1 的NaCl溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:先根据物质的量浓度的概念求出Cl-浓的物质的量浓度.根据溶液中Cl-的物质的量浓度=盐的浓度×化学式中氯离子个数,与溶液体积无关.
解答:
解:将0.1mol的KCl和0.1mol的AlCl3溶于水配成100mL混合溶液,Cl-物质的量浓度是
=4mol?L-1;
A、3 mol?L-1的NaCl溶液中c(Cl-)=3mol?L-1,
B、2mol?L-1的FeCl3溶液中c(Cl-)=2mol?L-1×3=6mol?L-1;
C、2mol?L-1的MgCl2溶液中c(Cl-)=2 mol?L-1×2=4mol?L-1;
D、2mol?L-1的NaCl溶液中c(Cl-)=2mol?L-1;
故选C.
| 0.1mol+0.1mol×3 |
| 0.1L |
A、3 mol?L-1的NaCl溶液中c(Cl-)=3mol?L-1,
B、2mol?L-1的FeCl3溶液中c(Cl-)=2mol?L-1×3=6mol?L-1;
C、2mol?L-1的MgCl2溶液中c(Cl-)=2 mol?L-1×2=4mol?L-1;
D、2mol?L-1的NaCl溶液中c(Cl-)=2mol?L-1;
故选C.
点评:本题考查了溶液中氯离子物质的量浓度的计算,难度不大,溶液中氯离子的物质的量浓度为盐的浓度与化学式中离子个数的积,与溶液的体积无关.

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目
下列变化的叙述中,不属于蛋白质变性的是( )
| A、动物的皮经过药剂鞣制后,变成柔软坚韧的皮革 |
| B、打针前用医用酒精对皮肤消毒 |
| C、蛋白质溶液里加入食盐变浑浊 |
| D、用福尔马林溶液浸泡动物标本 |
某二价金属的碳酸盐和酸式碳酸盐的混合物,跟足量的稀盐酸反应,消耗H+和生成CO2物质的量之比为6:5,则该混合物中碳酸盐和酸式碳酸盐的物质的量之比是( )
| A、1:1 | B、1:2 |
| C、1:3 | D、1:4 |
常温下,将0.1mol?L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
| A、溶液的pH增加 |
| B、CH3COOH电离度变大 |
| C、溶液的导电能力减弱 |
| D、溶液中c(OH-)减小 |
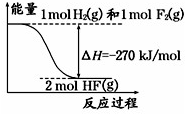 已知:H2(g)+F2(g)═2HF(g) 的能量变化如图所示,下列有关叙述中正确的是( )
已知:H2(g)+F2(g)═2HF(g) 的能量变化如图所示,下列有关叙述中正确的是( )| A、氟化氢气体分解生成氢气和氟气的反应是放热反应 |
| B、1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ |
| C、在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 |
| D、断裂1 mol H-H键和1 mol F-F 键放出的能量大于形成2 mol H-F键放出的能量 |
下列叙述正确的是( )
| A、全部由非金属元素形成的物质也可能含有离子键 |
| B、阴离子都只有还原性 |
| C、与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
| D、金属只能在溶液中发生置换反应 |
核内中子数为N的R2+离子,质量数为A,则n g它的氧化物RO中所含质子的物质的量是( )
A、
| ||
B、
| ||
| C、(A-N+2)mol | ||
D、
|
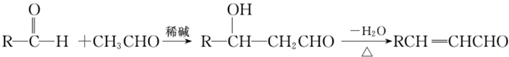
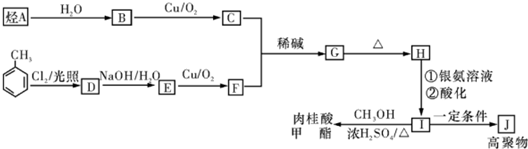
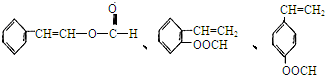 、
、