题目内容
有机物在反应中,常有下列原子间的共价键全部或部分断裂,如C-H、C-C、C=C、C-O、C═O等.下列各反应中,反应物分子中断裂键的排列,正确的组合是( )
| 化学反应 | 乙醇酯化 | 乙醇氧化 | 乙醛氧化 | 油脂皂化 | 多肽水解 |
| A | O-H | C-H | C-H | C-O | C-N |
| B | O-H | O-H | O-H | C-O | C-H |
| C | C-O | C-O | C-H | C═O | C═O |
| D | C-O | C-H | C-C | C-O | N-H |
| A、A | B、B | C、C | D、D |
考点:有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:乙醇酯化为羟基的取代,乙醇氧化生成乙醛,乙醛氧化为-CHO的氧化,油脂皂化为-COOC的水解,多肽水解为肽键的水解,以此来解答.
解答:
解:乙醇酯化为羟基的取代,O-H键断裂;
乙醇氧化生成乙醛,C-H和O-H键断裂;
乙醛氧化为-CHO的氧化,C-H键断裂;
油脂皂化为-COOC的水解,C-O键断裂;
多肽水解为肽键的水解,C-N键断裂;
故选A.
乙醇氧化生成乙醛,C-H和O-H键断裂;
乙醛氧化为-CHO的氧化,C-H键断裂;
油脂皂化为-COOC的水解,C-O键断裂;
多肽水解为肽键的水解,C-N键断裂;
故选A.
点评:本题考查有机物的结构与性质,侧重有机物反应的考查,注意把握官能团与性质的关系来分析解答,题目难度不大.

练习册系列答案
相关题目
在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )
| A、所用NaOH已经潮解 |
| B、向容量瓶中加水未到刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、所用容量瓶不干燥 |
下列表示的是有机化合物结构式中的一部分,其中不是官能团的是( )
| A、-OH |
B、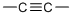 |
C、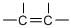 |
| D、-CH3 |
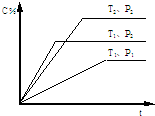 已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,下图表示在不同反应时间t 时,温度T和压强P与生成物C在混合物中的体积百分含量的关系曲线.由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,下图表示在不同反应时间t 时,温度T和压强P与生成物C在混合物中的体积百分含量的关系曲线.由曲线分析,下列判断正确的是( )| A、T1<T2,P1>P2,m+n>p,正反应吸热 |
| B、T1>T2,P1<P2,m+n>p,正反应放热 |
| C、T1<T2,P1>P2,m+n<p,正反应放热 |
| D、T1>T2,P1<P2,m+n<p,正反应吸热 |
某烃的结构简式为CH3-CH2-CH=C(C2H5)-C≡CH分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为( )
| A、4、3、5 |
| B、4、3、6 |
| C、2、5、4 |
| D、4、6、4 |
下列过程中,最终的白色沉淀不一定是BaSO4的是( )
A、Fe(NO3)2
| ||||||
B、Ba(NO3)2溶液
| ||||||
C、无色溶液
| ||||||
D、无色溶液
|
A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、NaHSO4溶液和BaCl2溶液中的一种,已知A、B溶液的pH相同,A、C混合后溶液变浑浊.下列说法不正确的是( )
| A、D溶液的pH>7 |
| B、C溶液中的溶质溶于水促进了水的电离 |
| C、溶液A滴入到碳酸氢钠溶液中产生气体 |
| D、溶液B与NaOH共热有气体产生 |
PH3在常温下是无色有大蒜气味的气体,它的分子呈三角锥形,以下关于PH3的叙述中正确的是( )
| A、PH3是非极性分子 |
| B、PH3中有孤电子对 |
| C、PH3是一种强氧化剂 |
| D、PH3分子中P-H键是非极性键 |