题目内容
(1)某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验.请回答下列问题:
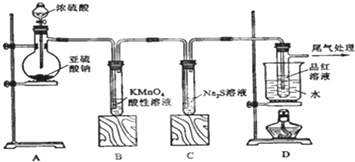
①实验过程中装置B、C发生的现象分别说明SO2具有的性质是 性和 性
配平装置B中发生反应的离子方程式
SO2+ MnO4-+ H2O-- Mn2++ SO42-+ H+
②装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象 ;
③尾气可采用 溶液吸收.
(2)在实验室欲制取适量的NO气体.
①NO通常用什么方法收集
②下列中最适宜完成该实验的简易装置是 (填序号);

③根据所选的装置依次写出所用试剂
④根据所选的装置,写出装置B的作用 .

①实验过程中装置B、C发生的现象分别说明SO2具有的性质是
配平装置B中发生反应的离子方程式
②装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象
③尾气可采用
(2)在实验室欲制取适量的NO气体.
①NO通常用什么方法收集
②下列中最适宜完成该实验的简易装置是

③根据所选的装置依次写出所用试剂
④根据所选的装置,写出装置B的作用
考点:性质实验方案的设计,二氧化硫的化学性质
专题:实验题
分析:(1)利用二氧化硫与高锰酸钾与硫化钠的溶液的氧化还原反应反应来分析;根据氧化还原反应中的电子守恒来配平方程式;
②根据二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色来解答;
③二氧化硫属于酸性气体,可以和碱之间反应,据此回答;
(2)①根据一氧化氮的性质确定收集方法;
②稀硝酸和铜反应制取一氧化氮无需加热,NO易与空气中氧气反应,则应用排水法收集,据此回答;
③根据稀硝酸和铜反应制取一氧化氮、用排水法收集来回答;
④一氧化氮用排水法收集,B的作用是收集产生的气体.
②根据二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色来解答;
③二氧化硫属于酸性气体,可以和碱之间反应,据此回答;
(2)①根据一氧化氮的性质确定收集方法;
②稀硝酸和铜反应制取一氧化氮无需加热,NO易与空气中氧气反应,则应用排水法收集,据此回答;
③根据稀硝酸和铜反应制取一氧化氮、用排水法收集来回答;
④一氧化氮用排水法收集,B的作用是收集产生的气体.
解答:
解:(1)①高锰酸钾溶液为紫红色,具有氧化性,二氧化硫具有还原性,二者发生氧化还原反应,此时体现二氧化硫的还原性,二氧化硫进入硫化钠溶液中发生的氧化还原反应为2S2-+SO2+2H2O=3S↓+4OH-,则观察到出现黄色浑浊,B中S元素的化合价升高,表现还原性,高锰酸钾和二氧化硫的反应中,Mn元素的化合价降低了5价,硫元素的化合价升高了2价,根据电子守恒,则S元素的前边系数是5,Mn元素的前边系数是2,根据元素守恒、电荷守恒,氢离子前边是4,水的前边系数是2,即2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+,
故答案为:还原;氧化;5、2、2、2、5、5;
②因二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色,则操作为待品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,观察到的现象为无色溶液恢复为红色,故答案为:操作:待品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热;现象:无色溶液恢复为红色;
③二氧化硫属于酸性气体,可以和碱NaOH之间反应,可以用氢氧化钠来进行尾气处理,故答案为:NaOH;
(2)①NO易与空气中氧气反应,则应用排水法收集,故答案为:排水法;
②稀硝酸和铜反应制取一氧化氮,NO易与空气中氧气反应,则应用排水法收集,收集时进气管较短,则应选择I装置,
故答案为:I;
③稀硝酸和铜反应制取一氧化氮,I装置中A加入稀硝酸和铜,为气体发生装置,B为气体的收集装置,用排水法收集,C为接受B中排出的水的装置,故答案为:稀硝酸和铜、水;
④B为气体的收集装置,用排水法收集,收集时进气管较短,故答案为:收集产生的NO.
故答案为:还原;氧化;5、2、2、2、5、5;
②因二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色,则操作为待品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,观察到的现象为无色溶液恢复为红色,故答案为:操作:待品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热;现象:无色溶液恢复为红色;
③二氧化硫属于酸性气体,可以和碱NaOH之间反应,可以用氢氧化钠来进行尾气处理,故答案为:NaOH;
(2)①NO易与空气中氧气反应,则应用排水法收集,故答案为:排水法;
②稀硝酸和铜反应制取一氧化氮,NO易与空气中氧气反应,则应用排水法收集,收集时进气管较短,则应选择I装置,
故答案为:I;
③稀硝酸和铜反应制取一氧化氮,I装置中A加入稀硝酸和铜,为气体发生装置,B为气体的收集装置,用排水法收集,C为接受B中排出的水的装置,故答案为:稀硝酸和铜、水;
④B为气体的收集装置,用排水法收集,收集时进气管较短,故答案为:收集产生的NO.
点评:本题考查制备实验的设计,题目难度中等,本题注意把握实验方法,结合物质的性质判断装置的选择.注意一氧化氮难溶于水,用排水法收集时进气管较短.

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目
如图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述正确的是( )
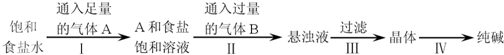

| A、A气体是CO2,B气体是NH3 |
| B、第Ⅲ步得到的晶体是Na2CO3?10H2O |
| C、第Ⅱ步的离子方程式为Na++NH3?H2O+CO2═NaHCO3↓+NH4+ |
| D、第Ⅳ步操作的主要过程有溶解、蒸发、结晶 |
从加热氯酸钾与MnO2的混合物制氧气后的剩余物中回收二氧化锰的操作顺序正确的是( )
| A、溶解、过滤、蒸发、洗涤 |
| B、溶解、过滤、洗涤、烘干 |
| C、溶解、蒸发、洗涤、过滤 |
| D、溶解、洗涤、过滤、烘干 |
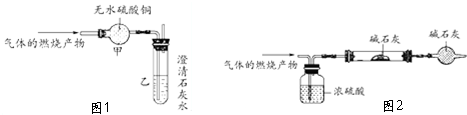
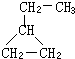 可表示为
可表示为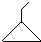 ,则金刚乙烷、金刚乙胺的结构简式可用下图表示.
,则金刚乙烷、金刚乙胺的结构简式可用下图表示.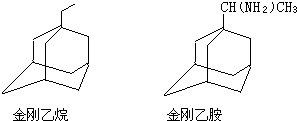
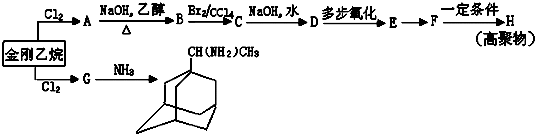
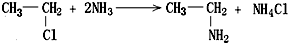
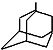 ,如金刚乙烷表示为R-CH2CH3)
,如金刚乙烷表示为R-CH2CH3)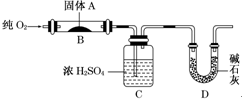 实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出)H:1 O:16 C:12
实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出)H:1 O:16 C:12