题目内容
离子键的强弱对离子化合物的熔、沸点有较大影响,一般来说,离子键越强,离子化合物的熔、沸点越高,而影响离子键强弱的因素有:离子的半径和电荷.离子半径越小,所带电荷数越多,离子键就越强,现有Cl、O、K、Na几种元素.
(1)写出上述元素形成离子中半径最大的离子的电子式: ;
(2)写出上述元素的离子形成的离子键最强的化合物的电子式: ;
(3)写出上述元素的离子形成的化合物中熔、沸点最低的化合物的电子式: .
(1)写出上述元素形成离子中半径最大的离子的电子式:
(2)写出上述元素的离子形成的离子键最强的化合物的电子式:
(3)写出上述元素的离子形成的化合物中熔、沸点最低的化合物的电子式:
考点:化学键,电子式,离子键的形成
专题:
分析:(1)电子层越多,半径越大,Cl、K的离子具有相同的电子排布,原子序数大的离子半径小;
(2)影响离子键强弱的因素有:离子的半径和电荷.离子半径越小,所带电荷数越多,离子键就越强,则氧化钠中离子键最强;
(3)离子形成的化合物中,离子半径越大,离子键越弱,熔、沸点越低.
(2)影响离子键强弱的因素有:离子的半径和电荷.离子半径越小,所带电荷数越多,离子键就越强,则氧化钠中离子键最强;
(3)离子形成的化合物中,离子半径越大,离子键越弱,熔、沸点越低.
解答:
解:电荷数最大的为氧元素,离子半径为Cl->K+>O2->Na+,
(1)电子层越多,半径越大,Cl、K的离子具有相同的电子排布,原子序数大的离子半径小,则Cl-的离子半径最大,其电子式为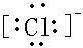 ,
,
故答案为: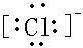 ;
;
(2)影响离子键强弱的因素有:离子的半径和电荷.离子半径越小,所带电荷数越多,离子键就越强,则氧化钠中离子键最强,则氧化钠的电子式为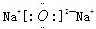 ,故答案为:
,故答案为: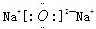 ;
;
(3)离子形成的化合物中,离子半径越大,离子键越弱,熔、沸点越低,则KCl的离子键最弱,其电子式为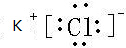 ,
,
故答案为: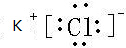 .
.
(1)电子层越多,半径越大,Cl、K的离子具有相同的电子排布,原子序数大的离子半径小,则Cl-的离子半径最大,其电子式为
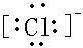 ,
,故答案为:
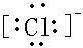 ;
;(2)影响离子键强弱的因素有:离子的半径和电荷.离子半径越小,所带电荷数越多,离子键就越强,则氧化钠中离子键最强,则氧化钠的电子式为
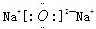 ,故答案为:
,故答案为: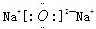 ;
;(3)离子形成的化合物中,离子半径越大,离子键越弱,熔、沸点越低,则KCl的离子键最弱,其电子式为
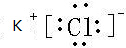 ,
,故答案为:
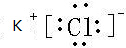 .
.
点评:本题考查化学键及离子键的形成,为高频考点,把握习题中的信息及离子半径与离子键的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
向20mL0.1moL?L-1的NH4HSO4溶液中滴0.1mol?L-1 NaOH溶液到恰好完全反应,正确的是( )
| A、整个反应过程中:c(H+)+c(Na+ )+c(NH4+)=c(OH-)+2c(SO42-) |
| B、滴入30mLNaOH溶液时(pH>7):c(NH4+)>c(NH3?H2O)>c(OH-)>c(H+) |
| C、当滴入20mLNaOH溶液时:2c(SO42-)=c(NH4+)+c(NH3?H2O) |
| D、当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)=c(OH-) |
短周期元素R的最高价氧化物对应的水化物的化学式HXROy,气态氢化物的化学式为HzR(或RHz),已知1molHXROy比1molHzR质量多64g,下列说法不正确的是( )
| A、有多种元素符合本题条件 |
| B、符合本题的HXROy 分子有一元酸和多元酸 |
| C、Z=X |
| D、R可能是第二周期元素 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
| W | X | |
| Y | Z |
| A、X元素形成的单核阴离子还原性强于Y |
| B、Z元素氧化物对应水化物的酸性一定强于Y元素氧化物对应水化物 |
| C、X、Y、Z中氢化物稳定性最弱的是Y的氢化物 |
| D、Z元素单质在化学反应中只表现氧化性 |
27g金属铝与1L 2mol?L-1NaOH溶液充分反应,生成的气体在标准状况下的体积为( )
| A、11.2L |
| B、22.4L |
| C、33.6L |
| D、44.8L |
浓硫酸是实验室必备的重要试剂,下列有关它的说法不正确的是( )
| A、具有强腐蚀性 |
| B、能使蔗糖变黑 |
| C、能用于干燥氨气 |
| D、加热时能与铜发生反应 |
氯化镉(CdCl2)是一种常用于薄膜太阳能电池上的物质,由于它有毒,科学家选用了另一种盐来替代它.这种替代物质是 ( )
| A、Cl2 |
| B、HCl |
| C、MgCl2 |
| D、Mg(OH)2 |
 .现有分子式C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生下图所示的一系列反应:
.现有分子式C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生下图所示的一系列反应:


 它的合成路线流程图合成路线流程图示例如下:CH3CH2OH
它的合成路线流程图合成路线流程图示例如下:CH3CH2OH