题目内容
根据下列某些短周期元素中元素性质的有关句回答问题.
(1)元素①、②和⑧的第一电离能由大到小的顺序是 (填元素符号);元素③、⑥和⑨的氢化物中沸点由高到低的顺序是 (填化学式).
(2)元素⑤、⑥和⑦的某两种元素形成的化合物中,每个原子都 满足最外层为8电子稳定结构的物质是 (写化学式).
(3)某元素R的原子半径为1.02×10-10m,它与钠形成Na2R2,其化学键类型有 ,其电子式是 (R用元素符号表示).
(4)元素①和⑨形成阳离子,其结构式为 ,其中心原子以 杂化轨道成键.
(5)元素⑤的原子基态电子排布式为 .
(6)元素②和⑦形成晶体的部分结构可用下图中的 来表示(填序号).

| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径/10-10m | 0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | +3 | +4 | +5 | +7 | +1 | +5 | ||
| 最低价态 | -1 | -2 | -4 | -3 | -1 | -3 | -1 |
(2)元素⑤、⑥和⑦的某两种元素形成的化合物中,每个原子都 满足最外层为8电子稳定结构的物质是
(3)某元素R的原子半径为1.02×10-10m,它与钠形成Na2R2,其化学键类型有
(4)元素①和⑨形成阳离子,其结构式为
(5)元素⑤的原子基态电子排布式为
(6)元素②和⑦形成晶体的部分结构可用下图中的

考点:晶胞的计算,原子核外电子排布,元素电离能、电负性的含义及应用,化学键,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:①②⑧最高正价都是+1,处于ⅠA族,原子半径①<⑧<②,则①为H、②为Na、⑧为Li;⑦⑩都有最低价-1,则处于ⅦA族,⑩没有正化合价,⑦为Cl、⑩为F;⑥⑨都有最高正价+5,处于ⅤA族,原子半径⑥>⑨,则⑥为P、⑨为N;③只有最低负价-2,则③为O;④只有最高正价+3,处于ⅢA族,原子半径大于磷原子,则④为Al;⑤有最高正价+4、最低负极-4,处于ⅣA族,原子半径小于氯原子,则⑤为C,据此解答.
解答:
解:①②⑧最高正价都是+1,处于ⅠA族,原子半径①<⑧<②,则①为H、②为Na、⑧为Li;⑦⑩都有最低价-1,则处于ⅦA族,⑩没有正化合价,⑦为Cl、⑩为F;⑥⑨都有最高正价+5,处于ⅤA族,原子半径⑥>⑨,则⑥为P、⑨为N;③只有最低负价-2,则③为O;④只有最高正价+3,处于ⅢA族,原子半径大于磷原子,则④为Al;⑤有最高正价+4、最低负极-4,处于ⅣA族,原子半径小于氯原子,则⑤为C,
(1)同主族自上而下第一电离能降低、非金属性越强第一电离能越大,故第一电离能H>Li>Na;
元素③、⑥和⑨的氢化物分别为H2O、NH3、PH3,常温下水是液体,沸点最高,NH3分子之间存在氢键,沸点高于PH3,故沸点H2O>NH3>PH3,
故答案为:H>Li>Na;H2O>NH3>PH3;
(2)元素C、N和Cl的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质是CCl4、PCl3,故答案为:CCl4、PCl3;
(3)某元素R的原子半径为1.02×10-10m,它与钠形成Na2R2,R为S元素,其电子式为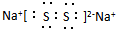 ,含有离子键、共价键,故答案为:离子键、共价键;
,含有离子键、共价键,故答案为:离子键、共价键; ;
;
(4)元素①和⑨形成阳离子为NH4+,其结构式为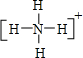 ,其中心N原子成4个N-H键,以sp3杂化轨道成键,故答案为:
,其中心N原子成4个N-H键,以sp3杂化轨道成键,故答案为: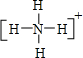 ;sp3;
;sp3;
(5)元素⑤为C,核外电子数为6,其原子基态电子排布式为1s22s22p2,故答案为:1s22s22p2;
(6)元素②和⑦形成晶体为NaCl,属于离子化合物,其晶胞结构中每个钠离子周围有6个氯离子、每个氯离子周围有6规格钠离子,A图符合其结构,故答案为:A.
(1)同主族自上而下第一电离能降低、非金属性越强第一电离能越大,故第一电离能H>Li>Na;
元素③、⑥和⑨的氢化物分别为H2O、NH3、PH3,常温下水是液体,沸点最高,NH3分子之间存在氢键,沸点高于PH3,故沸点H2O>NH3>PH3,
故答案为:H>Li>Na;H2O>NH3>PH3;
(2)元素C、N和Cl的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质是CCl4、PCl3,故答案为:CCl4、PCl3;
(3)某元素R的原子半径为1.02×10-10m,它与钠形成Na2R2,R为S元素,其电子式为
 ,含有离子键、共价键,故答案为:离子键、共价键;
,含有离子键、共价键,故答案为:离子键、共价键; ;
;(4)元素①和⑨形成阳离子为NH4+,其结构式为
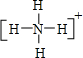 ,其中心N原子成4个N-H键,以sp3杂化轨道成键,故答案为:
,其中心N原子成4个N-H键,以sp3杂化轨道成键,故答案为: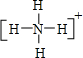 ;sp3;
;sp3;(5)元素⑤为C,核外电子数为6,其原子基态电子排布式为1s22s22p2,故答案为:1s22s22p2;
(6)元素②和⑦形成晶体为NaCl,属于离子化合物,其晶胞结构中每个钠离子周围有6个氯离子、每个氯离子周围有6规格钠离子,A图符合其结构,故答案为:A.
点评:本题考查元素周期表与元素周期律、常用化学用语、杂化轨道、晶胞结构等,难度中等,根据化合价与原子半径推断元素是解题关键,注意识记中学常见晶胞结构.

练习册系列答案
相关题目
设NA为伏加德罗常数的值,下列说法正确的是( )
| A、58.5g NaCl晶体中含有NA个氯化钠分子 |
| B、标准状况下,33.6L CH2O含有的分子数为1.5NA |
| C、78g苯分子中含有的碳碳双键数目为3NA |
| D、含有23g乙醇的水溶液中氢原子数为3NA |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温常压下,4.6g乙醇中含有C-H键的个数为0.6NA |
| B、一定温度下,15g甲醛和乙酸的混合物中O原子数为0.5NA |
| C、1mol Cl2和1mol H2O充分反应,生成的H+离子数为NA |
| D、标准状况下,11.2L庚烷完全燃烧后生成的CO2分子数为3.5NA |
在一定温度下,某浓度的硝酸与金属铜反应,生成NO2和NO的物质的量之比为l:3,则要使1mol Cu完全反应,需HNO3的物质的量为( )
| A、2.8 mol |
| B、2.6 mol |
| C、2.4 mol |
| D、O.8 mol |
在下列各组溶液中,离子间一定能大量共存的是( )
| A、pH=1的溶液:K+、Cu2+、Br-、SO42- |
| B、含有0.1mol/LI-的溶液:NH3+、Fe3+、SO42-、Cl- |
| C、含有0.1mol/LHCO3-的溶液:Na+、Al3+、NO3-、OH- |
| D、强酸性溶液:K+、Mg2+、NO3-、ClO- |

 钴(Co)是一种重要的战略金属,钴及其合金广泛应用于电机、机械、化工、航空和航天等领域.钴在化合物中通常以+2、+3的形式存在.
钴(Co)是一种重要的战略金属,钴及其合金广泛应用于电机、机械、化工、航空和航天等领域.钴在化合物中通常以+2、+3的形式存在.