题目内容
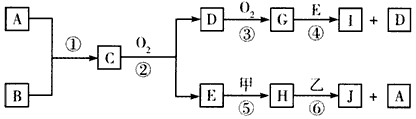
甲、乙为单质,丙为氧化物,它们存在如下关系:![]()
(1)若甲、乙均为非金属,满足条件的甲、乙可能是___________、___________。(列举常见的两组)
(2)若甲为金属,乙为非金属,甲、丙反应的化学方程式为:
____________________________________________________________________
(3)若甲、乙均为金属,甲、丙反应的化学方程式为
_____________________________________________________________________
(1)C Si(或C H2)
(2)2Mg+CO2![]() 2MgO+C或3Fe+4H2O
2MgO+C或3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
(3)2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
解析:所给反应“甲+丙![]() 乙+丁”为置换反应。
乙+丁”为置换反应。
(1)甲、乙均为非金属的置换反应有SiO2+![]() Si+2CO、H2O(g)+C
Si+2CO、H2O(g)+C![]() H2+CO、2H2S+O2====S↓+2H2O、
H2+CO、2H2S+O2====S↓+2H2O、![]() 2MgO+C、3Fe+4H2O
2MgO+C、3Fe+4H2O![]() Fe3O4+4H2、2Na+2H2O====2NaOH+H2↑等。(3)甲、乙均为金属的置换反应有Fe+CuSO4====Cu+FeSO4、Fe2O3+2Al
Fe3O4+4H2、2Na+2H2O====2NaOH+H2↑等。(3)甲、乙均为金属的置换反应有Fe+CuSO4====Cu+FeSO4、Fe2O3+2Al![]() 2Fe+Al2O3等。
2Fe+Al2O3等。

练习册系列答案
相关题目