题目内容
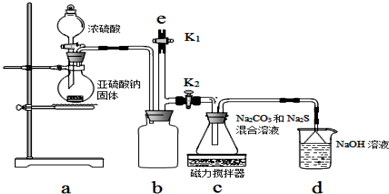
8.实验室用浓硫酸和乙醇反应制备乙烯,若温度过高或加热时间过长,制得的乙稀往往混有CO2、SO2、H2O(气体少量).请回答下列问题:(1)试分析CO2和SO2是怎么样产生的?乙醇或乙烯与浓硫酸发生氧化还原反应生成CO2和SO2 (用一句话说明).
(2)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g),按气流的方向,各装置的连接顺序是:④②①③.
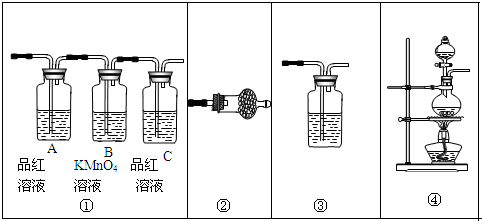
(3)实验时若观察到:①中从左到右A瓶中品红溶液褪色,B瓶中高锰酸钾溶液颜色逐渐变浅,C瓶中品红溶液不褪色,则A瓶的作用是检验是否有SO2,B瓶的作用是除去或吸收SO2,C瓶的作用是检验SO2是否除尽.
(4)装置②中所加的试剂名称是无水硫酸铜,它可以验证的气体是水蒸气,简述确定装置②在整套装置中的位置的理由是①③导出的气体带有水蒸气,影响水蒸气的确定.
(5)装置③中所盛溶液的名称是澄清的石灰水,它可以用来验证的气体是CO2.
分析 (1)浓硫酸有强氧化性,乙醇或乙烯与浓硫酸发生氧化还原反应生成CO2和SO2 ;
(2)二氧化硫是否存在可用品红溶液检验.检验二氧化碳可以用澄清石灰水溶液.检验水用无水硫酸铜,应先检验水蒸气的存在,不能先通过澄清的石灰水来检验二氧化碳的存在,应先通过品红溶液褪色检验SO2的存在;
(3)(4)(5)二氧化硫是否存在可用品红溶液检验.检验二氧化碳可以用澄清石灰水溶液.检验水用无水硫酸铜,
应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,二氧化碳的检验应放在排除SO2的干扰后进行,先通过品红溶液褪色检验SO2的存在;再通过酸性高锰酸钾溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净.最后用澄清石灰水实验检验二氧化碳.
解答 解:(1)浓硫酸有强氧化性,乙醇或乙烯与浓硫酸发生氧化还原反应生成CO2和SO2 ,
故答案为:乙醇或乙烯与浓硫酸发生氧化还原反应生成CO2和SO2 ;
(2)二氧化硫是否存在可用品红溶液检验.检验二氧化碳可以用澄清石灰水溶液.检验水用无水硫酸铜;应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,二氧化碳的检验应放在排除SO2的干扰后进行,选通过品红溶液褪色检验SO2的存在;再通过酸性高锰酸钾溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净.最后用澄清石灰水实验检验二氧化碳,
故答案为:④②①③;
(3)二氧化硫是否存在可用品红溶液检验.二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,二氧化碳的检验应放在排除SO2的干扰后进行,先通过品红溶液褪色检验SO2的存在;再通过酸性高锰酸钾溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,
故答案为:检验是否有SO2;除去或吸收SO2;检验SO2是否除尽;
(4)检验水用无水硫酸铜,白色变为蓝色说明含有水蒸气.验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气,应最先用用无水硫酸铜检验水,
故答案为:无水硫酸铜;水蒸气; ①③导出的气体带有水蒸气,影响水蒸气的确定;
(5)检验二氧化碳可以用澄清石灰水溶液,在排除二氧化硫的干扰后,澄清石灰水变浑浊,说明含有二氧化碳,
故答案为:澄清的石灰水;CO2.
点评 本题考查乙烯的化学性质、制备以及常见气体的检验,明确乙烯、浓硫酸的性质是解题关键,题目难度中等,注意实验原理及检验的先后顺序.

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案| A. | 原子半径:X>Y>Z>Q>W | |
| B. | 最高价氧化物对应的水化物的酸性:Z<Q | |
| C. | Q和W可形成原子个数比为1:1和1:2的化合物 | |
| D. | X、Y和W三种元素形成的化合物的水溶液呈碱性 |
查阅相关资料,得到主要试剂及产物的性质:
| 物质 | 相对分子质量 | 性质 |
| 废饮料瓶碎片 | 聚对苯二甲酸乙二醇酯:乳白色或浅黄色的聚合物. | |
| 乙二醇(EG) | 62 | 无色无臭液体,对动物有毒性.沸点:196~198℃,与水混溶. |
对苯二甲酸(TPA) | 166 | 白色晶体或粉末,低毒.弱酸.300℃以上升华.不溶于水、乙醚、氯仿等大多数有机溶剂,可溶于DMF等强极性有机溶剂. |
(一)解聚
实验装置如图所示,A为三颈烧瓶,B为直形冷凝管,C为吸滤芯瓶,各接口均为玻璃接口.向装置中加入一定量废饮料瓶碎片及辅助试剂(催化剂、水等).缓慢搅拌,加热.待温度计上的温度显示高出200℃时,停止加热.则:
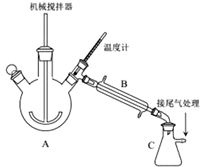
(1)写出聚对苯二甲酸乙二醇酯解聚的化学反应方程式:
 .
.(2)C中收集到的是乙二醇;C装置吸滤瓶不能(填“能”或“不能”)换页成敞口锥形瓶,原因:乙二醇有毒,不能直接排放到空气中.
(3)成品聚对苯二甲酸乙二酯是一种结晶性好,无色透明,极为坚韧的材料.有玻璃的外观,无臭、无味、无毒,易燃,燃烧时,产生蓝色边缘的黄色火焰.其燃烧反应属于D.
A.聚合反应 B.加成聚合反应
C.综合聚合反应 D.高分子化学反应
(4)工业上生产“PET”的反应式为:
 ,生产时,若消耗EG的物质的量比TPA多4‰,则上述聚合物的链节数n为250.
,生产时,若消耗EG的物质的量比TPA多4‰,则上述聚合物的链节数n为250. | A. | 主族元素的电负性越大,元素原子的第一电离能一定越大 | |
| B. | 在元素周期表中,元素电负性从左到右越来越小 | |
| C. | 在形成化合物时,电负性越小的元素越容易显正价 | |
| D. | 金属元素的电负性一定小于非金属元素的电负性 |
| A. | 称量样品→加热→冷却→称量CuO | |
| B. | 称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量 | |
| C. | 称量样品→加热→冷却→称量Cu(NO3)2 | |
| D. | 称量样品→加NaOH→过滤→加热→冷却→称量CuO |

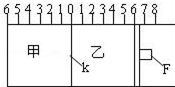 Ⅰ.如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题:
Ⅰ.如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题: