题目内容
下列溶液,一定呈中性的是( )
| A、由等体积、等物质的量浓度的一元酸跟NaOH溶液混合后所形成的溶液 | ||
| B、c(H+)=1.0×10-7mol?L-1的溶液 | ||
| C、pH=7的溶液 | ||
D、c(H+)=
|
考点:水的电离,盐类水解的应用
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:溶液的酸碱性是根据溶液中H+浓度与OH-浓度的相对大小判断,不能直接根据溶液的pH进行判断,
当c(H+)>c(OH-),溶液就呈酸性;
当c(H+)=c(OH-),溶液就呈中性;
当溶液中c(H+)<c(OH-),溶液就呈碱性;据此进行判断.
当c(H+)>c(OH-),溶液就呈酸性;
当c(H+)=c(OH-),溶液就呈中性;
当溶液中c(H+)<c(OH-),溶液就呈碱性;据此进行判断.
解答:
解:A.由等体积、等物质的量浓度的一元酸溶液与NaOH溶液混合后,酸如果为弱酸,则反应后溶液显示碱性,若酸为强酸,则反应后溶液为中性,故A错误;
B.c(H+)=10-7mol?L-1的溶液,溶液的pH=7,pH=7的溶液不一定呈中性,如100℃时,水的离子积常数是10-12,当PH=6时溶液呈中性,当PH=7时溶液呈碱性,故B错误;
C.pH=7的溶液不一定呈中性,如100℃时,水的离子积常数是10-12,当PH=6时溶液呈中性,当PH=7时溶液呈碱性,故C错误;
D.c(H+)=
,即c(H+)=c(OH-),故溶液显中性,故D正确,
故选D.
B.c(H+)=10-7mol?L-1的溶液,溶液的pH=7,pH=7的溶液不一定呈中性,如100℃时,水的离子积常数是10-12,当PH=6时溶液呈中性,当PH=7时溶液呈碱性,故B错误;
C.pH=7的溶液不一定呈中性,如100℃时,水的离子积常数是10-12,当PH=6时溶液呈中性,当PH=7时溶液呈碱性,故C错误;
D.c(H+)=
| Kw |
故选D.
点评:本题主要考查溶液的酸碱性的判断,难度不大.注意不能根据溶液的PH值判断溶液的酸碱性,要根据氢离子浓度和氢氧根离子浓度的相对大小判断溶液的酸碱性.

练习册系列答案
相关题目
0.6mol的Cu2S与足量的稀HNO3反应,生成物为Cu(NO3)2、H2SO4、NO、H2O,则参加反应的被还原和未被还原的硝酸的物质的量分别为( )
| A、0.6mol、0.3mol |
| B、1.2mol、0.6mol |
| C、2mol、0.6mol |
| D、2mol、2.4mol |
下列关于反应热的说法正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B、CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol |
| C、甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 |
| D、需要加热才能发生的反应一定是吸热反应 |
如图是实验室用漂粉精固体【主要成分为Ca(ClO)2】和浓盐酸制备氯气并进行一系列相关实验的装置(夹持设备已略).下列叙述错误的是( )


| A、装置B中饱和食盐水的作用是除去氯气中的氯化氢气体 |
| B、通过装置B中锥形瓶及长颈漏斗的液面变化,可以监测实验过程中C是否发生堵塞 |
| C、装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ依次放入湿润的有色布条、无水氯化钙、干燥的有色布条 |
| D、设计装置D、E的目的是比较氯、溴、碘的非金属性,当向D中缓缓通入足量氯气后,打开活塞,将装置D中少量溶液加入装置E中,观察苯层为紫红色,可以说明溴的非金属性强于碘 |
 如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是( )
如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是( )| A、Janusene的分子式为C30H20 |
| B、Janusene不属于苯的同系物 |
| C、Janusene最多18个碳原子共面 |
| D、Janusene苯环上的一氯代物有4种 |
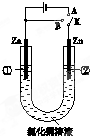 在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按图连接.
在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按图连接.