题目内容
5.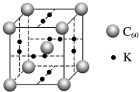 科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示.该化合物中的K原子和C60分子的个数比为( )
科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示.该化合物中的K原子和C60分子的个数比为( )| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
分析 先根据均摊法计算晶胞中K原子、C60分子数目,然后计算出该化合物中的K原子和C60分子的个数比.
解答 解:根据均摊法可知,该晶胞中K原子数目为:2×6×$\frac{1}{2}$=6,含有C60分子数目为:1+8×$\frac{1}{8}$=2,
所以该晶胞中K原子、C60分子数目之比=6:2=3:1,
故选C.
点评 本题考查了晶胞的计算,题目难度不大,明确均摊法的应用为解答关键,注意掌握常见晶胞结构特点,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
15.元素周期表的一部分,回答下列问题(用元素符号填写):
(1)分别写出①、③两种元素形成的高价态化合物的结构式O=C=O
(2)写出⑨的原子结构示意图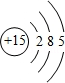 .
.
(3)在这些元素中,最活泼的金属元素的最高价氧化物对应水化物的电子式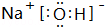 ,其溶于水时破坏的作用力为离子键
,其溶于水时破坏的作用力为离子键
(4)这些元素的最高价氧化物的对应水化物中酸性最强HClO4;形成的两性氢氧化物的化学式是Al(OH)3;上述两者反应的离子方程式Al(OH)3+3H+═Al3++3H2O
(5)从⑤到⑪的元素中,原子半径最小Cl.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VIIA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)写出⑨的原子结构示意图
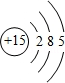 .
.(3)在这些元素中,最活泼的金属元素的最高价氧化物对应水化物的电子式
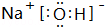 ,其溶于水时破坏的作用力为离子键
,其溶于水时破坏的作用力为离子键(4)这些元素的最高价氧化物的对应水化物中酸性最强HClO4;形成的两性氢氧化物的化学式是Al(OH)3;上述两者反应的离子方程式Al(OH)3+3H+═Al3++3H2O
(5)从⑤到⑪的元素中,原子半径最小Cl.
16.下表是元素周期表的一部分,回答下列有关问题:
(1)写出元素符号:①N(填化学式,下同)
(2)在这些元素中,最活泼的金属元素是K,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅤⅡA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
20.下列化学用语能正确表示相应意义的是( )
| A. | 丙烯的结构简式CH2CH2CH3 | B. | 四氯化碳的结构式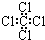 | ||
| C. | 丁烷的结构简式CH3(CH2)2CH3 | D. | 苯的分子式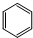 |
10.同周期的X、Y、Z三元素,其最高价氧化物水化物的酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4,则下列判断正确的是( )
| A. | 原子半径 X>Y>Z | |
| B. | 非金属性 X>Y>Z | |
| C. | X、Y、Z的单质与氢气化合能力由弱到强 | |
| D. | 气态氢化物的稳定性按X、Y、Z的顺序由弱到强 |
17.下列关于能量转换的认识不正确的是( )
| A. | 手机电池在充电时,电能转变为化学能 | |
| B. | 绿色植物进行光合作用时,太阳能主要转化为化学能 | |
| C. | 煤燃烧时,化学能主要转化为热能 | |
| D. | 白炽灯工作时,电能全部转化为光能 |
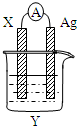 依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.
依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.
 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应.
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应. ,C的分子式C2H5Cl,D的结构简式CH3CH2OH.
,C的分子式C2H5Cl,D的结构简式CH3CH2OH. .
.