题目内容
 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.(1)下列说法正确的是
A.化学变化中的能量变化主要由化学键变化引起的
B.放热反应发生时不一定要加热,但吸热反应必须要加热才能发生
C.钢铁的吸氧腐蚀和析氢腐蚀的负极反应都为Fe-2e-=Fe2+
D.CaCO3(s)═CaO(s)+CO2(g)△H=+178.5KJ?mol-1的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5KJ的热量
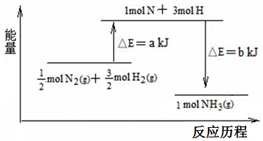
(2)101kPa条件下,氮气和氢气反应生成氨气的能量变化示意图如图:
已知:①a=1127;②b=1219
则:1mol N2和3mol H2参与反应生成2mol NH3
考点:反应热和焓变
专题:化学反应中的能量变化
分析:(1)A、化学反应的实质是旧件的断裂和新键的生成;
B、放热反应发生时不一定要加热,吸热反应不一定加热才能发生;
C、金属腐蚀的实质都是金属失电子的氧化反应过程;
D、物质的分解过程是吸热的过程;
(2)反应热=反应物中的键能之和-生成物中的键能之和,根据反应物和产物能量高低判断反应热的正负.
B、放热反应发生时不一定要加热,吸热反应不一定加热才能发生;
C、金属腐蚀的实质都是金属失电子的氧化反应过程;
D、物质的分解过程是吸热的过程;
(2)反应热=反应物中的键能之和-生成物中的键能之和,根据反应物和产物能量高低判断反应热的正负.
解答:
解:(1)A、化学反应的实质是旧件的断裂和新键的生成,化学变化中的能量变化主要由化学键变化引起的,故A正确;
B、放热反应发生时不一定要加热,如氧化钙和水之间的反应,吸热反应不一定加热才能发生,如氯化铵和氢氧化钡晶体之间的反应,故B错误;
C、金属腐蚀的实质都是金属失电子的氧化反应过程,负极反应都为Fe-2e-=Fe2+,故C正确;
D、碳酸钙的分解过程是吸热的过程,即1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要吸收178.5KJ的热量,故D错误.
故选AC;
(2)根据图示知道反应物的能量高于生成物的能量,所以该反应放热,反应热=反应物的键能-生成物的键能,氮气和氢气反应生成氨气的热化学方程式为:
N2(g)+
H2(g)=NH3(g)△H=a-bkJ?mol-1,则N2(g)+3H2 (g)=2NH3(g)△H=2(a-b)kJ?mol-1=2(1127-1219)kJ/mol=-184kJ?mol-1,
故答案为:放出;184.
B、放热反应发生时不一定要加热,如氧化钙和水之间的反应,吸热反应不一定加热才能发生,如氯化铵和氢氧化钡晶体之间的反应,故B错误;
C、金属腐蚀的实质都是金属失电子的氧化反应过程,负极反应都为Fe-2e-=Fe2+,故C正确;
D、碳酸钙的分解过程是吸热的过程,即1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要吸收178.5KJ的热量,故D错误.
故选AC;
(2)根据图示知道反应物的能量高于生成物的能量,所以该反应放热,反应热=反应物的键能-生成物的键能,氮气和氢气反应生成氨气的热化学方程式为:
| 1 |
| 2 |
| 3 |
| 2 |
故答案为:放出;184.
点评:本题考查学生热化学方程式的意义和化学反应的实质知识,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
相关题目
氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A、加入浓氢氧化钠溶液都产生红褐色沉淀 |
| B、都能发生丁达尔现象 |
| C、分散质颗粒直径都在l~100nm之间 |
| D、颜色都呈红褐色 |
1919年,科学家第一次实现了人类多年的梦想--人工转变元素.这个核反应如下:
N+
He→
O+
H,下列叙述正确的是( )
7 14 |
4 2 |
17 8 |
1 1 |
A、
 | ||
| B、氦气分子为双原子分子 | ||
C、一个H2
| ||
D、C
 |
两种金属的混和粉末15克,跟足量盐酸充分反应时,恰好得到11.2升氢气(标准状况),下列各组金属不能构成符合上述条件的混和物的是( )
| A、Mg和Ag |
| B、Al和Zn |
| C、Al和Fe |
| D、Mg和Al |


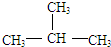 E、
E、 与
与
 如图是以石墨为电极电解CuCl2溶液的装置示意图.
如图是以石墨为电极电解CuCl2溶液的装置示意图.