题目内容
2.下列关于放射性元素说法正确的是( )①所有的元素都具有放射性;
②只有铀具有放射性;
③元素具有放射性是由原子内部结构变化引起的;
④放射性元素的放射现象不是自发的,需要外界条件(如光照)来引起的.
| A. | ①②③④ | B. | ③ | C. | ①②③ | D. | ①②④ |
分析 ①有些原子核不稳定,可以自发地衰变,放出粒子或射线,但不是所有元素都具有放射性;
②许多元素具有放射性,铀238核($\underset{\stackrel{238}{\;}}{92}\underset{\stackrel{\;}{U}}{\;}$)衰变时产生的新核钍234也具有放射性;
③原子由原子核和核外电子构成;
④某些元素具有天然放射现象.
解答 解:①不是所有的元素都具有放射性,如钠元素,无放射性,故①错误;
②不只有铀具有放射性,如某些花岗岩会产生具有放射性的氡$\underset{\stackrel{222}{\;}}{86}\underset{\stackrel{\;}{Rn}}{\;}$具有放射性,从而对人体产生伤害,故②错误;
③有的原子经过放射变化后,放射出了质子,变成了另一种元素的原子,某些原子具有放射性,放出中子,原子核未变,所以元素具有放射性是由原子内部结构变化引起的,故③正确;
④某些原子具有放射性,即原子能自动地放射出一些固定的粒子,如花岗岩会产生具有放射性的氡$\underset{\stackrel{222}{\;}}{86}\underset{\stackrel{\;}{Rn}}{\;}$具有放射性,故④错误;
故选B.
点评 本题考查元素的放射性,掌握元素具有放射性以及放射的产物进行分析是解答关键,题目难度不大.

练习册系列答案
相关题目
12.化学与生活密切相关,下列有关说法错误的是( )
| A. | 在人体内,油脂在脂肪酶催化作用下水解为高级脂肪酸和甘油 | |
| B. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| C. | 以液化石油气代替燃油可减少大气污染 | |
| D. | 医用消毒酒精中乙醇的浓度为95% |
13.在一定温度下,可逆反应2A (g)+B (g)?C (g)+D (g)达到平衡的标志是( )
| A. | C的生成速率和B的消耗速率相等 | |
| B. | 反应混合物中A、B、C、D的浓度不再发生变化 | |
| C. | 2v正(A)=v正(B) | |
| D. | v正(A)=2v正(B) |
17.下列有关物质的应用说法正确的是( )
| A. | 可以用铝制槽罐车运输浓硫酸 | |
| B. | 亚硝酸盐可以防腐,所以在食品中可以广泛使用 | |
| C. | 洁厕灵和漂白粉都具有去污作用,一同使用效果会更好 | |
| D. | 治疗胃酸过多可以使用碳酸钠 |
1.现有苯甲酸、苯酚溶于乙醇所得的混合液,某同学设计方案分离三种物质,并检验其中的某些离子和物质.
已知:(1)酸性强弱:HCl>苯甲酸>H2CO3>苯酚>HCO3-
(2)部分物理参数如下:
供选择试剂:10%氢氧化钠溶液、0.1mol/L盐酸、0.1mol/LNa2CO3、0.1mol/L NaHCO3、浓溴水、生石灰、0.1mol/L FeCl3、0.1mol/L BaCl2、CO2、0.1mol/L溴水、澄清石灰水
(1)分离物质流程如下:
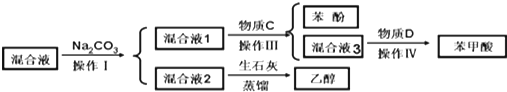
物质C是CO2,操作IV是过滤.
(2)操作III发生的主要化学反应方程式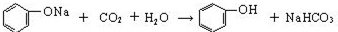 .
.
(3)混合液2中加入生石灰的原因是生石灰与混合液2中的水反应,生成氢氧化钙溶液,并放出热量,便于乙醇从混合物中蒸馏出.
(4)该同学检验混合液1中是否含有苯酚和NaHCO3,以证明酸性的强弱.完成下列各步实验及实验现象和结论.
(5)称取2.0g苯甲酸和苯酚的混合固体溶于足量乙醇中,滴加足量饱和NaHCO3溶液,测得放出的CO2(标准状况下,不考虑CO2溶于水)为33.6mL,则苯甲酸的质量分数为$\frac{\frac{0.036L}{22.4L/mol}×122g/mol}{2g}$×100%,(只列式,不计算),结果为9.2%.(结果保留1位小数)(苯甲酸的相对分子质量为122,苯酚相对分子质量为94)
已知:(1)酸性强弱:HCl>苯甲酸>H2CO3>苯酚>HCO3-
(2)部分物理参数如下:
| 密度 (g•mL-1) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 苯甲酸 | 1.2659 | 122.13 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
| 苯酚 | 1.07 | 40.6 | 181.9 | 易溶于乙醇、乙醚,65℃以上能与水互溶 |
| 乙醇 | 0.79 | -114.3 | 78.5 | 与水混溶,可混溶于醚、氯仿、甘油等多数有 机溶剂 |
(1)分离物质流程如下:

物质C是CO2,操作IV是过滤.
(2)操作III发生的主要化学反应方程式
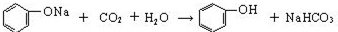 .
.(3)混合液2中加入生石灰的原因是生石灰与混合液2中的水反应,生成氢氧化钙溶液,并放出热量,便于乙醇从混合物中蒸馏出.
(4)该同学检验混合液1中是否含有苯酚和NaHCO3,以证明酸性的强弱.完成下列各步实验及实验现象和结论.
| 实验步骤 | 现象和结论 |
| ①取少量混合液1于试管,滴加BaCl2, 振荡,静置 | 产生白色沉淀,BaCO3 |
| ②取少量步骤①上层清夜于试管,滴加0.1mol/L盐酸再将产生的气体通入澄清石灰水中 | 澄清石灰水变浑浊 说明混合液1含有HCO3- |
| ③另取少量混合液1于试管,滴加0.1mol/L FeCl3溶液,振荡 | 溶液不显紫色, 说明混合液1不含有酚羟基 |
8.下列说法正确的是( )
| A. | 4mol/LNaCl溶液与2mol/LNa2SO4溶液混合后,c(Na+)为4 mol/L | |
| B. | 240 g NaCl溶液中溶有40 g NaCl,该温度下NaCl的溶解度为20g | |
| C. | 22.4 L HCl气体溶于水制成1 L溶液,该溶液的物质的量浓度为1 mo1/L | |
| D. | 把5 g胆矾(CuSO4?5H2O)溶于45 g水中,所得溶液溶质的质量分数为10% |


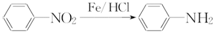 (苯胺,易被氧化)
(苯胺,易被氧化)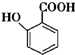 不可选用的试剂有c(填标号).
不可选用的试剂有c(填标号).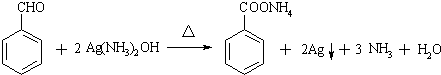 ;若F为高分子化合物,则反应⑦的化学方程式为n
;若F为高分子化合物,则反应⑦的化学方程式为n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$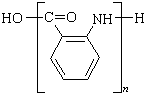 +(n-1)H2O.
+(n-1)H2O.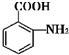 的合成路线流程图(无机试剂任用).合成路线流程图示例如下(已知
的合成路线流程图(无机试剂任用).合成路线流程图示例如下(已知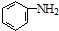 容易被氧化剂氧化):
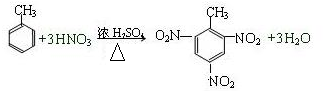
容易被氧化剂氧化):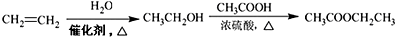 .
.
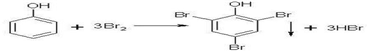 .
.