题目内容
11.将密度为1.84g/cm3、质量分数为98%的浓硫酸稀释成1000mL、物质的量浓度为2mol/L、密度为1.10g/cm3的稀硫酸.求:(1)所需浓硫酸的体积;
(2)所需水的体积.(水的密度可视为1g/cm3)(要求有计算过程.)
分析 (1)设需浓硫酸体积为V1,根据稀释前后硫酸的质量不变可得:V1×1.84g/cm3×98%=1.0L×2mol/L×98g/mol,据此计算出所需浓硫酸的体积;
(2)设需水的体积为V2,根据稀释前后质量不变,可得:1.0L×2mol/L×98g/mol+V2×1g/cm3=1000mL×1.10g/cm3,据此计算出所需水的体积.
解答 解:(1)设需浓硫酸体积为V1,根据稀释前后硫酸的质量不变可得:
V1×1.84g/cm3×98%=1.0L×2mol/L×98g/mol,
解得:V1=108.7mL,
答:所需浓硫酸的体积为108.7mL;
(2)设需水的体积为V2,
根据稀释前后质量不变,可得:1.0L×2mol/L×98g/mol+V2×1g/cm3=1000mL×1.10g/cm3,
解得:V2=904mL,
答:所需水的体积为904mL.
点评 本题考查了物质的量浓度的计算、溶液稀释的有关计算,题目难度中等,明确物质的量与物质的量浓度之间的关系为解答关键,注意掌握质量守恒定律在化学计算中的应用方法.

练习册系列答案
相关题目
1.下列化学用语表示正确的是( )
| A. | 原子核中有7个中子的碳原子:12C | |
| B. | 明矾的电离方程式是:KAl(SO4)2•12H2O═K++Al3++2SO42-+12H2O | |
| C. | K+结构示意图: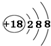 | |
| D. | Ba(OH)2与H2SO4反应的化学方程式是:Ba(OH)2+H2SO4═BaSO4↓+H2O |
2.下列叙述不正确的是( )
| A. | 强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 | |
| B. | 影响化学平衡常数的因素是温度 | |
| C. | 放热反应不一定能自发进行,而吸热反应也可能自发进行 | |
| D. | 熵增大的反应其焓变一定增大,焓变增大的反应其熵不一定增大 |
6.下列叙述正确的是( )
| A. | 摩尔是国际上规定的七个基本物理量之一 | |
| B. | 一定温度、压强下,气体体积由其物质的量的多少决定 | |
| C. | 不同的气体,若体积不等,则它们所含的分子数一定不等 | |
| D. | 体积为22.4L的O2,其质量可能为32g |
16.可用于区别溴蒸气与二氧化氮气体的试剂是( )
①淀粉碘化钾溶液②水③AgNO3溶液④NaOH溶液.
①淀粉碘化钾溶液②水③AgNO3溶液④NaOH溶液.
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③④ |
3.蕙可用作杀虫剂、杀菌剂和汽油阻凝剂,其结构简式为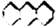 .其二氯代物的同分异构体共有(不考虑立体异构)( )
.其二氯代物的同分异构体共有(不考虑立体异构)( )
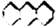 .其二氯代物的同分异构体共有(不考虑立体异构)( )
.其二氯代物的同分异构体共有(不考虑立体异构)( )| A. | 14种 | B. | 15种 | C. | 16种 | D. | 17种 |
17.下列反应的离子方程式书写正确的是( )
| A. | 氯化铝溶液中加人过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 向1molFeBr2溶液中通入 1.5molCl2 :2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 氯化亚铁溶液中通人氯气:Fe2++Cl2═Fe3++2C1- |
18.下列饱和溶液中通入过量的CO2气体,溶液不会变挥浊的是( )
| A. | NaAlO2溶液 | B. | Na2SiO3溶液 | C. | 苯酚钠溶液 | D. | CaCl2溶液 |