题目内容
4.下列物质之间的转化都能一步实现的是( )| A. | Si→SiO2→H2SiO3→Na2SiO3 | B. | Al→Al2O3→Al(OH)3→NaAl(OH)4 | ||
| C. | N2→NH3→NO→NO2→HNO3→NO2 | D. | S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
分析 A、二氧化硅无法一步转化为硅酸;
B、氧化铝无法一步转化为氢氧化铝;
C、氮气与氢气合成氨气,氨催化氧化生成一氧化氮,一氧化氮氧化成二氧化氮,二氧化氮与水反应生成硝酸,浓硝酸与铜生成二氧化氮;
D、硫在氧气中燃烧生成二氧化硫.
解答 解:A、二氧化硅不溶于水,而且不与水反应,所以二氧化硅无法一步转化为硅酸,故A错误;
B、氧化铝不溶于水,也不与水反应,所以氧化铝无法一步转化为氢氧化铝,故B错误;
C、氮气与氢气合成氨气,氨催化氧化生成一氧化氮,一氧化氮氧化成二氧化氮,二氧化氮与水反应生成硝酸,浓硝酸与铜生成二氧化氮,所以能实现各步转化,故C正确;
D、硫在氧气中燃烧生成二氧化硫,不能实现一步转化,故D错误;
故选C.
点评 本题考查物质的转化,要熟练掌握元素及其化合物之间的转化关系,具有一定的难度,尤其是不能一步转化的反应要注意.

练习册系列答案
相关题目
15.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | pH=1的溶液:Ag+、Al3+、Cl-、SO42- | |
| B. | 能使酚酞试液变红的溶液:Na+、K+、HCO3-、S2- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10-12的溶液:NH4+、Cu2+、NO3-、Cl- | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液:K+、Fe2+、SO42-、NO3- |
12.室温下,下列溶液中粒子浓度关系正确的是( )
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液:c(OH-)═c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)═2c(CO32-)+c(OH-) | |
| D. | CH3COONa和CaCl2溶液:c(Na+)+c(Ca2+)═c(CH3COO-)+c(OH-)+c(Cl-) |
19.自然界各种原生铜的硫化物经氧化、淋滤后变成CuSO4溶液,并向深部渗透时,遇到闪锌矿(ZnS)和方铅矿(PbS),便慢慢地转变为铜蓝(CuS),下列有关该过程的解释及说法不合理的是( )
| A. | 原生铜的硫化物具有还原性 | |
| B. | 常温时ZnS、PbS、CuS都难溶于水,CuSO4可溶于水 | |
| C. | 铜蓝的形成过程是:ZnS(S)+Cu2+?CuS(S)+Zn2+ | |
| D. | 硝酸型酸雨不利于铜蓝的形成:CuS+2H+═Cu2++H2S↑ |
16.将纯锌片和纯铜片按图所示方式插入稀硫酸中一段时间,以下叙述正确的是( )


| A. | 铜片表面发生氧化反应 | B. | 电子从铜片流向锌片 | ||
| C. | 电流从锌片流向铜片 | D. | 锌片为负极铜片为正极 |
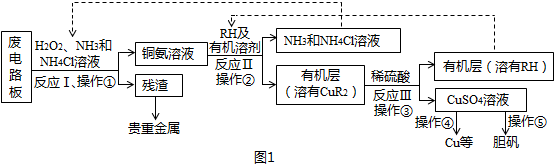
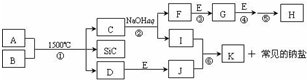 如图是一些常见元素的单质或化合物之间的转化关系.溶液中的水以及部分反应物或生成物未标出.A、E是空气中的两种主要成分,C是由两种元素组成的新型材料,并且C的原子数、最外层电子数之和与SiC相同,J是一种能引起温室效应的气体,K是两性化合物.反应③、④、⑤用于工业中生产H.
如图是一些常见元素的单质或化合物之间的转化关系.溶液中的水以及部分反应物或生成物未标出.A、E是空气中的两种主要成分,C是由两种元素组成的新型材料,并且C的原子数、最外层电子数之和与SiC相同,J是一种能引起温室效应的气体,K是两性化合物.反应③、④、⑤用于工业中生产H.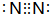 ,G的化学式NO;
,G的化学式NO;