题目内容
12. 元素铜在溶液中主要以[Cu(H2O)4]2+(天蓝色)、[Cu(OH)4]2-(蓝色)、[CuCl2]-、[Cu(NH3)4]2+(深蓝色)等形式存在.CuCl为难溶于水的白色固体.回答下列问题:
元素铜在溶液中主要以[Cu(H2O)4]2+(天蓝色)、[Cu(OH)4]2-(蓝色)、[CuCl2]-、[Cu(NH3)4]2+(深蓝色)等形式存在.CuCl为难溶于水的白色固体.回答下列问题:(1)在浓的强碱溶液中,Cu2+与Al3+的化学性质相似.在少量的CuSO4溶液中,逐渐加入浓的NaOH溶液直至过量,可观察到的现象是溶液天然色逐渐褪色,同时蓝色絮状沉淀生成,然后沉淀溶解形成蓝色溶液.
(2)CuCl溶于浓盐酸时发生的反应为CuCl+HCl?H[CuCl2],要从H[CuCl2]溶液中析出沉淀的方法是加水稀释.在热的CuCl2溶液中加入铜粉,可制得CuCl,其反应的离子方程式为Cu2++2Cl-+Cu$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl,但实际上该反应较难持续进行,其原因是生成的CuCl附着在铜粉的表面,影响反应继续进行,使反应彻底进行的操作是加入浓盐酸,使CuCl溶解生成[CuCl2]-.
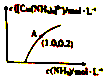
(3)[Cu(H2O)4]2+和[Cu(NH3)4]2+在溶液中可以相互转化.:t℃时,初始浓度为1mol•L-1的CuSO4溶液中{ Cu2+实际以[Cu(H2O)4]2+的形式存在},[Cu(NH3)4]2+的浓度随氨水浓度[c(NH3)]的变化如图所示
①CuSO4溶液与过量氨水发生反应的总的离子方程式为[Cu(H2O)4]2++4NH3?[Cu(NH3)4]2++4H2O.
②由图可知,溶液的酸性增大,[Cu(H2O)4]2+转化为[Cu(NH3)4]2+的平衡转化率减小(填“增大”“减小”或“不变”).根据A点数据,计算出该温度下的平衡常数K=0.25.
③升高温度,溶液中[Cu(H2O)4]2+的平衡转化率减小,则该反应的△H<(填“>”“<”或“=”)0
④硫酸四氯合铜{[Cu(NH3)4]SO4}在碱性镀铜工艺中常用作电镀液的主要成分,电镀时,要控制局部温度不得高于150℃,可能的原因是超过150℃,Cu(NH3)4]SO4易分解.电解时.阴极的电极反应式为[Cu(NH3)4]2++2e-=Cu↓+4NH3.
分析 (1)由于Cu2+与Al3+的化学性质相似,在少量的CuSO4溶液中,逐滴加入NaOH溶液后,先生成蓝色Cu(OH)2沉淀,继续滴加氢氧化钠溶液,蓝色Cu(OH)2沉淀溶解,得蓝色[Cu(OH)4]2-溶液;
(2)从H[CuCl2]溶液中析出沉淀加水稀释,在热的CuCl2溶液中加入铜粉,发生Cu+CuCl2=2CuCl,生成的CuCl附着在铜粉的表面,影响反应继续进行,使反应彻底进行,加入浓盐酸,使CuCl溶解生成[CuCl2]-;
(3)①CuSO4溶液与过量氨水发生反应生成深蓝色的[Cu(NH3)4]2+;
②由图可知,溶液的酸性增大,[Cu(H2O)4]2+转化为[Cu(NH3)4]2+的平衡转化率变小;化学平衡常数通常用各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值来表示;
③升高温度,平衡向吸热的方向移动;
④超过150℃,Cu(NH3)4]SO4易分解,电解时.阴极得电子发生还原反应.
解答 解:(1)元素铜在溶液中主要以[Cu(H2O)4]2+(天蓝色)存在,由于Cu2+与Al3+的化学性质相似,在少量的CuSO4溶液中,逐滴加入NaOH溶液后,发生反应:Cu2++2OH-=Cu(OH)2↓,先生成蓝色Cu(OH)2沉淀,继续滴加氢氧化钠溶液,蓝色Cu(OH)2沉淀溶解,得蓝色[Cu(OH)4]2-溶液,反应为:Cu(OH)2+2OH-?[Cu(OH)4]2-(蓝色),
故答案为:溶液天然色逐渐褪色,同时蓝色絮状沉淀生成,然后沉淀溶解形成蓝色溶液;
(2)CuCl溶于浓盐酸时发生的反应为:CuCl+HCl?H[CuCl2],该反应为可逆反应,CuCl为难溶于水的白色固体,要从H[CuCl2]溶液中析出沉淀的方法,加水稀释,平衡逆向移动,析出CuCl,在热的CuCl2溶液中加入铜粉,可制得CuCl,离子方程式为:Cu2++2Cl-+Cu$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl,因生成的CuCl附着在铜粉的表面,实际上该反应较难持续进行,使反应彻底进行,加入浓盐酸,使CuCl溶解生成[CuCl2]-,
故答案为:加水稀释;Cu2++2Cl-+Cu$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl;生成的CuCl附着在铜粉的表面,影响反应继续进行;加入浓盐酸,使CuCl溶解生成[CuCl2]-;
(3)①CuSO4溶液与过量氨水发生反应:[Cu(H2O)4]2++4NH3?[Cu(NH3)4]2++4H2O,
故答案为:[Cu(H2O)4]2++4NH3?[Cu(NH3)4]2++4H2O;
②[Cu(NH3)4]2+的浓度随氨水浓度变大变大,溶液的酸性增大,[Cu(H2O)4]2+转化为[Cu(NH3)4]2+的平衡转化率变小,A点(1.0,0.2),
[Cu(H2O)4]2++4NH3?[Cu(NH3)4]2++4H2O,
始 1mol/L
变 0.2mol/L
终 0.8mol/L 1.0mol/L 0.2mol/L
平衡常数K,=$\frac{0.2mol/L}{0.8mol/L×(1.0mol/L)^{4}}$=0.25,
故答案为:减小;
③升高温度,平衡向吸热的方向移动,溶液中[Cu(H2O)4]2+的平衡转化率减小,说明正反应为放热,即△H<0,
故答案为:<;
④电镀时,超过150℃,可能发生3[Cu(NH3)4]SO4$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+8NH3↑+2N2↑+3SO2↑+6H2O,所以要控制局部温度不得高于150℃,电解时.阴极[Cu(NH3)4]2+得电子发生还原反应:[Cu(NH3)4]2++2e-=Cu↓+4NH3,
故答案为:超过150℃,Cu(NH3)4]SO4易分解;[Cu(NH3)4]2++2e-=Cu↓+4NH3.
点评 本题考查物质结构有关知识,掌握铜及其化合物的性质以及配合物知识是解答关键,题目难度中等.

| A. | SO2+2NaOH═Na2SO3+H2O | B. | 3NO2+2H2O═2HNO3+NO | ||
| C. | 3Fe+4H2O(g) $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 | D. | 2Na+2H2O═2NaOH+H2↑ |
| A. | 空气中的分子质量变大 | B. | 空气中的分子间隔变小 | ||
| C. | 空气中的分子种类改变 | D. | 空气中的分子数目变少 |
| A. | V3>V2>V1 | B. | V1>V2=V3 | C. | V3>V2=V1 | D. | V1=V2>V3 |
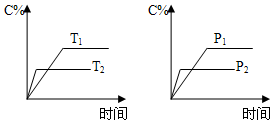 可逆反应aA(s)+bB(g)?cC(g)+dD(g)进行过程中,当其他条件不变时,C的体积分数C%与温度(T)、压强(P)的关系如图所示.下列叙述正确的是( )
可逆反应aA(s)+bB(g)?cC(g)+dD(g)进行过程中,当其他条件不变时,C的体积分数C%与温度(T)、压强(P)的关系如图所示.下列叙述正确的是( )| A. | 达到平衡后,加入催化剂,C的体积分数增大 | |
| B. | 达到平衡后,升高温度,平衡向左移动 | |
| C. | 化学方程式中,b>c+d | |
| D. | 达到平衡后,增加A的量,平衡向右移动 |
| A. | 1.5 mol NO2与足量的H2O反应,转移的电子数为NA | |
| B. | 常温常压下,0.5NA个CO2分子质量为22 g | |
| C. | 1 mol/L的CH3COOH中CH3COO-的浓度小于1 mol/L,而1 mol/L CH3COONa中CH3COO-等于1 mol/L | |
| D. | 18g 18O2中含有的中子数为10NA |