题目内容
已知A为中学化学中的一种盐,B、C为日常生活中常见的金属,离子有相同化合价.通常条件下D为无色无味气体,无色气体G遇空气变红棕色.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如图(部分反应产物已略去).
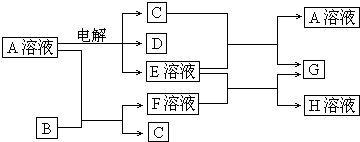
请回答下列问题:
(1)A的化学式为 .
(2)A溶液与Na2O2反应的总化学方程式为 .
(3)E的稀溶液与F溶液反应的离子方程式为 .
(4)若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体,则滤液中溶质的物质的量浓度为 .(假设溶液体积不变)

请回答下列问题:
(1)A的化学式为
(2)A溶液与Na2O2反应的总化学方程式为
(3)E的稀溶液与F溶液反应的离子方程式为
(4)若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体,则滤液中溶质的物质的量浓度为
考点:无机物的推断
专题:推断题
分析:根据题意,采用正推和逆推相结合的方法推断,电解A溶液时产生金属单质C和另外一种气体D,应为电解含氧酸盐溶液,在阴极上析出不活泼金属,则C应为铜,D为氧气,E溶液能与C金属发生氧化还原反应,且E溶液与F溶液也能反应生成无色无味气体G,说明E溶液具有强氧化性,应为硝酸,故A为硝酸铜,C为铜,D为氧气,G为NO,F与硝酸反应生成NO,说明且含有金属B元素,说明F溶液具有还原性,应为Fe(NO3)2溶液,B为Fe,H为Fe(NO3)3,由此可回答(1)(3)题;Na2O2与水反应生成NaOH和氧气,加入到Cu(NO3)2溶液中有蓝色沉淀生成;根据电解硝酸铜的电极方程式:2Cu(NO3)2+2H2O
2Cu+O2↑+4HNO3,可计算溶液的PH;根据化学方程式,利用质量守恒定律计算硝酸铜的物质的量,进而计算溶液的物质的量浓度.
| ||
解答:
解:(1)电解A溶液时产生金属单质C和另外一种气体D,应为电解含氧酸盐溶液,在阴极上析出不活泼金属,则C应为铜,D为氧气,E溶液能与C金属发生氧化还原反应,且E溶液与F溶液也能反应生成无色无味气体G,说明E溶液具有强氧化性,应为硝酸,故A为硝酸铜,C为铜,D为氧气,G为NO,F与硝酸反应生成NO,说明且含有金属B元素,说明F溶液具有还原性,应为Fe(NO3)2溶液,B为Fe,H为Fe(NO3)3,故答案为:Cu(NO3)2;
(2)Na2O2与水加入到Cu(NO3)2溶液中反应生成NaOH和氧气,NaOH和Cu(NO3)2反应生成蓝色沉淀2Cu(OH)2,方程式为2Na2O2+2Cu(NO3)2+2H2O=2Cu(OH)2↓+4NaNO3+O2↑,
故答案为:2Na2O2+2Cu(NO3)2+2H2O=2Cu(OH)2↓+4NaNO3+O2↑;
(3)硝酸具有强氧化性,Fe2+具有还原性,二者发生氧化还原反应,反应的离子方程式为3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O;
(4)向盐A溶液中加入金属单质B,反应的化学方程式为:Fe+Cu(NO3)2═Fe(NO3)2+Cu,
Fe+Cu(NO3)2═Fe(NO3)2+Cu△m
1mol 8g
n 10.16g-10g=0.16g
n=
=0.02mol,所以溶液的浓度为:
=0.2mol/L,
故答案为:0.2 mol/L.
(2)Na2O2与水加入到Cu(NO3)2溶液中反应生成NaOH和氧气,NaOH和Cu(NO3)2反应生成蓝色沉淀2Cu(OH)2,方程式为2Na2O2+2Cu(NO3)2+2H2O=2Cu(OH)2↓+4NaNO3+O2↑,
故答案为:2Na2O2+2Cu(NO3)2+2H2O=2Cu(OH)2↓+4NaNO3+O2↑;
(3)硝酸具有强氧化性,Fe2+具有还原性,二者发生氧化还原反应,反应的离子方程式为3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O;
(4)向盐A溶液中加入金属单质B,反应的化学方程式为:Fe+Cu(NO3)2═Fe(NO3)2+Cu,
Fe+Cu(NO3)2═Fe(NO3)2+Cu△m
1mol 8g
n 10.16g-10g=0.16g
n=
| 0.16 |
| 8 |
| 0.02mol |
| 0.1L |
故答案为:0.2 mol/L.
点评:本题以无机物的推断为载体,为高频考点,侧重于学生的分析能力的考查,考查电化学知识和溶液的有关计算,具有一定难度,根据框图,推断出各种物质是做好本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关说法中正确的是( )
| A、烧瓶、锥形瓶、量筒加热时均需垫上石棉网 |
| B、新制氯水保存在棕色细口瓶中,并放在阴凉处 |
| C、将蓝色硫酸铜晶体放入浓硫酸属于物理变化 |
| D、化石燃料属于可再生能源,不影响可持续发展 |
下列物质中能水解,且最终产物为两种有机物的是( )
| A、葡萄糖 | B、淀粉 |
| C、蔗糖 | D、纤维素 |
下列现象或事实可用同一原理解释的是( )
| A、铁分别加入浓硫酸和氢氧化钠溶液中均无明显现象 |
| B、SO2既能使品红褪色也能使酸性高锰酸钾褪色 |
| C、漂白粉溶液和硅酸钠溶液久置空中都变质 |
| D、H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率 |
下列说法中正确的是( )
| A、0.1mol/L(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| B、pH=4的醋酸稀释l0倍,溶液中c(CH3COOH)、c(OH-)均减小 |
| C、常温下向CH3COONa溶液中加入适量CH3COOH溶液,使混合液的pH=7,则混合液中c(Na+)=c(CH3COO-) |
| D、等浓度的弱酸HA溶液和NaOH溶液等体积混合,所得混合液显碱性 |
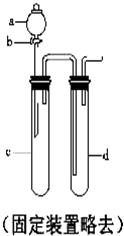 铜与稀硝酸反应产生NO,NO又被氧化成NO2,对实验观察无色NO有干扰,过多的NO、NO2又会污染环境,改进实验的涉及符合绿色化学的思想.有兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”的实验,以探究化学实验的绿色化.
铜与稀硝酸反应产生NO,NO又被氧化成NO2,对实验观察无色NO有干扰,过多的NO、NO2又会污染环境,改进实验的涉及符合绿色化学的思想.有兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”的实验,以探究化学实验的绿色化.