题目内容
9.已知第六周期稀有气体的原子序数是86,则第82号元素在周期表中的位置为第六周期、ⅣA族.分析 第六周期稀有气体的原子序数是86,85号元素为ⅤⅡA族,84号元素为ⅥA族,则82号元素处于ⅣA族元素,据此判断该元素在周期表中的位置.
解答 解:第六周期稀有气体的原子序数是86,则82号元素处于第二周期;
周期表中与稀有气体相邻的85号元素处于ⅤⅡA族,84号元素处于ⅥA族,则82号元素处于ⅣA族,
所以82元素位于周期表中ⅣA族,
故答案为:第六周期、ⅣA族.
点评 本题考查了元素周期表结构及其应用,题目难度不大,明确原子结构与元素在元素周期表中的位置关系为解答关键,注意掌握判断元素在周期表中位置的方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
19.下列说法错误的是( )
| A. | SiO2是沙子的主要成分,纯净的SiO2是光纤制品的基本原料 | |
| B. | 水晶的基本结构单元是[SiO4]四面体结构 | |
| C. | 将游离态的氮转变为氮的化合物就是氮的固定,合成氨是一种人工固氮方法 | |
| D. | 将等物质的量的氯气和二氧化硫同时通入品红溶液中,褪色比二氧化硫通入品红溶液快 |
17.下列叙述中,不能用勒夏特列原理解释的是( )
| A. | 合成氨需用铁触媒加快反应速率 | |
| B. | 高压比常压有利于合成SO3的反应 | |
| C. | 由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 | |
| D. | 收集氯气可用排饱和食盐水法 |
4. (1)在已知存在H2、Cl2、I2、HCl和Hl的时代,根据原子通过共价键形成分子的基本特点(如下图),推测还可能存在的一种化合物(A),其化学式为ICl.
(1)在已知存在H2、Cl2、I2、HCl和Hl的时代,根据原子通过共价键形成分子的基本特点(如下图),推测还可能存在的一种化合物(A),其化学式为ICl.
(2)请在下表中用相应的化学方程式表示出该化合物(A)可能具有的性质.
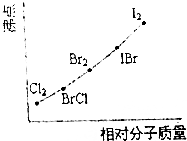
(3)图是部分卤素单质和XX′型卤素互化物的沸点与其相对分子质量的关系图.它们的沸点随着相对分子质量的增大而升高.其原因是分子晶体的熔沸点随分子量的增大而升高.试推测化合物(A)的沸点所处的最小范围Br2<ICl<IBr(用有关物质代表沸点数据).
 (1)在已知存在H2、Cl2、I2、HCl和Hl的时代,根据原子通过共价键形成分子的基本特点(如下图),推测还可能存在的一种化合物(A),其化学式为ICl.
(1)在已知存在H2、Cl2、I2、HCl和Hl的时代,根据原子通过共价键形成分子的基本特点(如下图),推测还可能存在的一种化合物(A),其化学式为ICl. | H- | Cl- | I- | |
| -H | H-H | H-Cl | H-I |
| -Cl | H-Cl | Cl-Cl | |
| -I | H-I | I-I |
| 反应物 | 化合物(A) | Br2 |
| Na | 2Na+Br2=2NaBr | |
| H2 | H2+Br2=2HBr | |
| H2O | H2O+Br2?HBr+HBrO | |
| Kl | 2Kl+Br2=I2+2KBr |
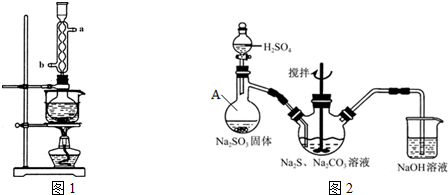
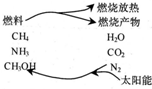
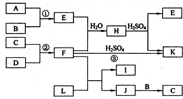 图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.(b)反应①、②是化工生产中的重要反应.(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.(e)化合物J由两种元素组成,其相对分子质量为32.
图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.(b)反应①、②是化工生产中的重要反应.(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.(e)化合物J由两种元素组成,其相对分子质量为32.