题目内容
12.下列有关离子的检验方法一定正确的是( )| A. | 向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含Ag+ | |
| B. | 向某溶液中滴加KSCN溶液,若溶液出现血红色则说明原溶液中含Fe3+ | |
| C. | 向某溶液中滴加足量稀HCl,产生的气体能使澄清石灰水变浑浊,则说明原溶液中一定含CO32- | |
| D. | 加入硝酸钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,则说明原溶液中一定有离子SO42- |
分析 A.滴入氯化钡溶液生成白色沉淀,加稀硝酸后沉淀不溶解,可能是生成硫酸钡沉淀或氯化银沉淀;
B.滴加KSCN溶液呈红色,说明存在铁离子;
C.滴入稀盐酸能生成气体的可能是碳酸根离子、碳酸氢根离子、亚硫酸根离子、亚硫酸氢根离子;
D.亚硫酸钡沉淀中加入硝酸会转化为硫酸钡沉淀,据此回答.
解答 解:A.滴加稀硝酸后滴入氯化钡溶液生成白色沉淀,不能排除硫酸根离子结合钡离子生成硫酸钡白色沉淀,沉淀可能是生成硫酸钡沉淀或氯化银沉淀,不一定是银离子,故A错误;
B.滴加KSCN溶液呈红色,原溶液一定含Fe3+,故B正确;
C.和稀盐酸发生反应生成气体的离子可以是CO32-、HCO3-、SO32-、HSO3-,不一定是CO32-,故C错误;
D.加入硝酸钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,则说明原溶液中一定有亚硫酸根离子或是硫酸根离子中的至少一种离子,故D错误;
故选B.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质为解答关键,注意熟练掌握常见离子的检验方法,试题侧重基础知识的考查,培养了学生得到灵活应用能力.

练习册系列答案
相关题目
1.下列叙述中,正确的是( )
| A. | 含金属元素的离子一定都是阳离子 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 金属阳离子被还原不一定得到金属单质 | |
| D. | 某元素从化合态变为游离态时,该元素一定被还原 |
2.化合物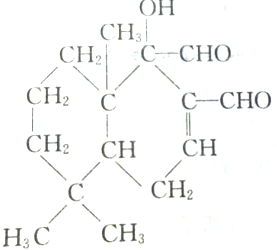 所含官能团有( )
所含官能团有( )
 所含官能团有( )
所含官能团有( )| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
19.下列物质中不含非极性共价键的是( )
①Na2O2 ②CCl4 ③HCN ④CH2=CH2 ⑤CH3COOH ⑥NaOH.
①Na2O2 ②CCl4 ③HCN ④CH2=CH2 ⑤CH3COOH ⑥NaOH.
| A. | ①②③④ | B. | ④⑤⑥ | C. | ②③⑤⑥ | D. | ①③⑤ |
7.下列说法正确的是( )
| A. | 加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+ | |
| B. | 向某溶液中滴加稀盐酸,生成的无色无味气体能使澄清的石灰水变浑浊,则原溶液中一定含有CO32- | |
| C. | 加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO42- | |
| D. | 向Ca(ClO)2溶液通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 |
17.以葡萄糖为燃料的微生物燃料电池结构示意图如图,关于该电池的叙述不正确的是( )
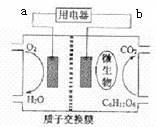

| A. | 微生物促进了反应中电子的转移 | |
| B. | 连接a的电极为负极 | |
| C. | 放电过程中,质子(H+)从负极区向正极区迁移 | |
| D. | 电池的负极反应为:C6H12O6+6H2O-24e-═6CO2+24H+ |
1.下列有机物命名正确的是( )
| A. | CH3-CH═CH-CH3 二丁烯 | B. | 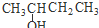 2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3OOCC2H5 乙酸乙酯 | D. | CH3CH(CH3)CH2COOH 3-甲基丁酸 |